题目内容
实验室有一包粉末状物质。可能是氯化钠、硫酸钠、碳酸钠,氯化铁中的一种或几种组成,为了确定原粉末的成分,某校化学兴趣小组的同学按下图所示进行试验:
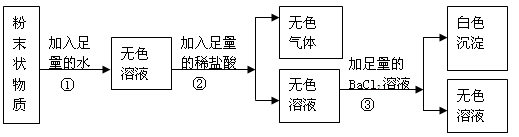
(1)该粉末中一定不含有的物质是 ,可能含有的物质是 。
(2)写出步骤③的化学方程式: 。

(1)该粉末中一定不含有的物质是 ,可能含有的物质是 。
(2)写出步骤③的化学方程式: 。
(1)氯化铁(1分); 氯化钠 (1分);
(2)Na2SO4 + BaCl2== BaSO4↓ + 2NaCl (1分)
(2)Na2SO4 + BaCl2== BaSO4↓ + 2NaCl (1分)
(1)加入水得到无色溶液,说明一定没有氯化铁;加入稀盐酸有无色气体,说明一定有碳酸钠;加入BaCl2溶液产生白色沉淀,说明一定含有硫酸钠,故不能确定是否含有氯化钠;故答案为:氯化铁氯化钠。
(2)硫酸钠与氯化钡反应生成硫酸钡白色沉淀和氯化钠,故其化学方程式为Na2SO4 + BaCl2== BaSO4↓ + 2NaCl 。
(2)硫酸钠与氯化钡反应生成硫酸钡白色沉淀和氯化钠,故其化学方程式为Na2SO4 + BaCl2== BaSO4↓ + 2NaCl 。

练习册系列答案
相关题目
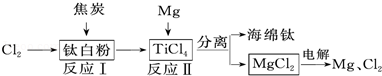
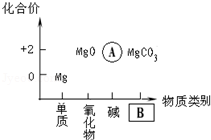
 Ti+2MgCl2.该反应在下列哪种环境中进行 _________ (填序号).
Ti+2MgCl2.该反应在下列哪种环境中进行 _________ (填序号). Ti+2MgCl2.若要制得24g钛,需要镁的质量是多少克?(写出计算过程) _________ .
Ti+2MgCl2.若要制得24g钛,需要镁的质量是多少克?(写出计算过程) _________ .