��Ŀ����
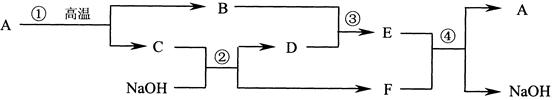
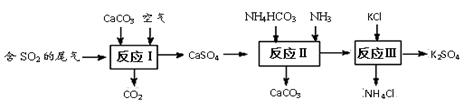
(7�֣�ij�Ȼ�����Ʒ�к��������Ȼ��ƺ��Ȼ�þ�������dz�ȥ�Ȼ�����Ʒ�������Ȼ��ƺ��Ȼ�þ�����̣�

��ش�
��1���Ȼ�����Ʒ���ᴿ
��KOH��Һ������ȥ��������������Ӧ�Ļ�ѧ����ʽ�� ��
�ڼ��롰�Լ�A���ɳ�ȥ�Ȼ�����Ʒ�е��Ȼ��ƣ���Ӧ�Ļ�ѧ����ʽ��
����֤�Ȼ�����ȫ����ȥ�ķ�����
��
�ۼ��롰�Լ�B����Ŀ���� ��
�ܡ�����1����Ҫ�õ����������������� ��
��2�����ᴿ��KCl��������200g10%��KCl��Һ����ҪKCl������Ϊ g������ʱ�����õ��IJ����������ձ����ιܡ��������� ��

��ش�
��1���Ȼ�����Ʒ���ᴿ
��KOH��Һ������ȥ��������������Ӧ�Ļ�ѧ����ʽ�� ��
�ڼ��롰�Լ�A���ɳ�ȥ�Ȼ�����Ʒ�е��Ȼ��ƣ���Ӧ�Ļ�ѧ����ʽ��
����֤�Ȼ�����ȫ����ȥ�ķ�����
��
�ۼ��롰�Լ�B����Ŀ���� ��
�ܡ�����1����Ҫ�õ����������������� ��
��2�����ᴿ��KCl��������200g10%��KCl��Һ����ҪKCl������Ϊ g������ʱ�����õ��IJ����������ձ����ιܡ��������� ��
��1����2KOH+ MgCl2 ="=" Mg(OH)2��+2KCl
��K2CO3+ CaCl2 ="=" CaCO3��+2KCl��ȡ������Һ�����ϲ���Һ�����Թ��У��μ�K2CO3
��Һ����û�а�ɫ�������֣���˵��CaCl2����ȫ����ȥ�����غŲ��ֻش���ȷ�Ÿ��֣�
�۳�ȥ������KOH��K2CO3��Һ�����KOH��K2CO3�������ʲŸ��֣�
�ܽ��裬��ֹҺ�ηɽ������غŲ��ֻش���ȷ�Ÿ��֣�
��2��20g����Ͳ
��K2CO3+ CaCl2 ="=" CaCO3��+2KCl��ȡ������Һ�����ϲ���Һ�����Թ��У��μ�K2CO3
��Һ����û�а�ɫ�������֣���˵��CaCl2����ȫ����ȥ�����غŲ��ֻش���ȷ�Ÿ��֣�
�۳�ȥ������KOH��K2CO3��Һ�����KOH��K2CO3�������ʲŸ��֣�
�ܽ��裬��ֹҺ�ηɽ������غŲ��ֻش���ȷ�Ÿ��֣�
��2��20g����Ͳ
��1���Ȼ�þ���������ط�Ӧ����������þ��ɫ�������Ȼ��أ��Ȼ�����̼��ط�Ӧ�����Ȼ��غ�̼��ư�ɫ��������ƽ���ɣ���֤�Ȼ�����ȫ����ȥ�ķ�����ȡ�ϲ���Һ���ټ���̼�����Һ�������г������ɣ����롰�Լ�B��ϡ�����Ŀ���ǣ��ѹ�����̼��س�ȥ���������У���������������ã���ֹ�ֲ��¶ȹ������Һ�ηɽ����ʴ�Ϊ����MgCl2+2KOH=Mg��OH��2��+2KCl����CaCl2+K2CO3=CaCO3��+2KCl��ȡ�ϲ���Һ���ټ���̼�����Һ�������г������ɣ��۰ѹ�����̼��س�ȥ���ܽ������ã���ֹ�ֲ��¶ȹ������Һ�ηɽ�
��2����ҪKCl������=200g��10%=20g������ʱ�����õ��IJ����������ձ����ιܡ�����������Ͳ���ʴ�Ϊ��20����Ͳ
��2����ҪKCl������=200g��10%=20g������ʱ�����õ��IJ����������ձ����ιܡ�����������Ͳ���ʴ�Ϊ��20����Ͳ

��ϰ��ϵ�д�
 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
�����Ŀ