题目内容
【题目】赤铜是一种铜的氧化物,因其外观与铜粉的颜色相似,故名“赤铜”。某兴趣小组欲确证草酸晶体的热分解产物,并测得赤铜的化学式,请你参与过程分析。
【资料】1.草酸晶体(H2C2O4·3H2O)在浓硫酸作用下受热分解,化学方程式为:
H2C2O43H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
2.浓硫酸具有吸水性,常用作气体干燥剂;无水硫酸铜遇水分变蓝色。
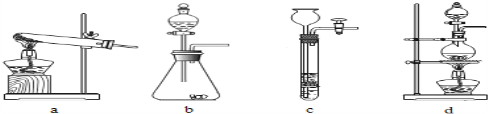
(1)下列可用作草酸分解制取气体的装置是 (填字母编号)
【问题讨论】
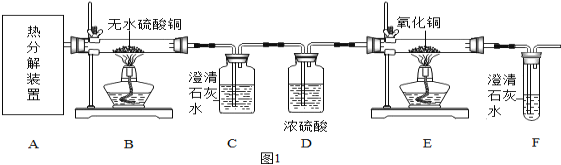
用上图所示装置进行实验(装置C中澄清石灰水足量):
(2)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是 。
(3)B装置的作用是 。证明草酸晶体的热分解产物中有CO2的现象是 ,该反应的化学方程式是 。
(4)从环保的角度考虑,该套实验装置明显的缺陷是 。
【数据分析与计算】
(5)称取7.2g赤铜样品(假设样品是纯净物),用上述实验装置进行实验,待赤铜完全反应后,测得E装置玻璃管内固体粉末的质量为6.4g,试计算确定赤铜的化学式(列式计算,2分)
(6)根据你求出的赤铜化学式,写出E装置中发生的化学方程式 。
【答案】(1)d(2)利用草酸热分解产生的气体排出装置中的空气,防止一氧化碳与空气混合,加热爆炸。(3)验证草酸热分解产物中有水 石灰水变浑浊
Ca﹙OH﹚2+CO2=CaCO3↓+H2O
(4)一氧化碳尾气未处理,会污染空气(5)Cu2O(6)CO+Cu2O=2Cu+CO2(反应条件加热)
【解析】
试题分析∶根据所学知识和题中信息知,赤铜是一种铜的氧化物,因其外观与铜粉的颜色相似,故名“赤铜”。某兴趣小组欲确证草酸晶体的热分解产物,并测得赤铜的化学式,请你参与过程分析。1.草酸晶体(H2C2O4·3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O![]() CO2↑+CO↑+4H2O.2.浓硫酸具有吸水性,常用作气体干燥剂;无水硫酸铜遇水分变蓝色。(1)下列可用作草酸分解制取气体的装置是d.用上图所示装置进行实验(装置C中澄清石灰水足量):(2)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是利用草酸热分解产生的气体排出装置中的空气,防止一氧化碳与空气混合,加热爆炸。(3)B装置的作用是验证草酸热分解产物中有水, 证明草酸晶体的热分解产物中有CO2的现象是石灰水变浑浊.该反应的化学方程式是Ca(OH) 2+CO2=CaCO3↓+H2O。(4)从环保的角度考虑,该套实验装置明显的缺陷是一氧化碳尾气未处理,会污染空气。【数据分析与计算】(5)称取赤铜赤铜样品(假设样品是纯净物),用上述实验装置进行实验,待赤铜完全反应后,测得E装置玻璃管内固体粉末的质量为6.4g,试计算确定赤铜的化学式∶生成铜质量6.4g,则赤铜赤铜样品含氧质量7.5g-6.4g=1.1g.设赤铜的化学式为CuxOy .64x∶16y=6.4g∶1.1g,x∶y=2∶1.赤铜的化学式∶Cu2O .
CO2↑+CO↑+4H2O.2.浓硫酸具有吸水性,常用作气体干燥剂;无水硫酸铜遇水分变蓝色。(1)下列可用作草酸分解制取气体的装置是d.用上图所示装置进行实验(装置C中澄清石灰水足量):(2)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是利用草酸热分解产生的气体排出装置中的空气,防止一氧化碳与空气混合,加热爆炸。(3)B装置的作用是验证草酸热分解产物中有水, 证明草酸晶体的热分解产物中有CO2的现象是石灰水变浑浊.该反应的化学方程式是Ca(OH) 2+CO2=CaCO3↓+H2O。(4)从环保的角度考虑,该套实验装置明显的缺陷是一氧化碳尾气未处理,会污染空气。【数据分析与计算】(5)称取赤铜赤铜样品(假设样品是纯净物),用上述实验装置进行实验,待赤铜完全反应后,测得E装置玻璃管内固体粉末的质量为6.4g,试计算确定赤铜的化学式∶生成铜质量6.4g,则赤铜赤铜样品含氧质量7.5g-6.4g=1.1g.设赤铜的化学式为CuxOy .64x∶16y=6.4g∶1.1g,x∶y=2∶1.赤铜的化学式∶Cu2O .
考点∶考查实验探究的基本思路和方法。

 阅读快车系列答案
阅读快车系列答案