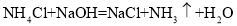题目内容
某沿海工业区排放的污水中含有少量的 Fe2+、Na+、Ca2+、Cu2+、Cl-,为了达到零污染的目标,将污水进行如下工业流程处理(已知:氢氧化亚铁是一种白色絮状沉淀物)

(1)步骤Ⅰ的操作名称是___________,写出步骤Ⅰ中的化学方程式:___________。
(2)滤渣Ⅰ所含的物质是________________(填化学式)。
(3)在滤液Ⅲ中加入盐酸使得到的溶液呈中性,要使用_______________来测定溶液的酸碱度,确保盐酸不过量。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某化学兴趣小组对厕所使用的洁厕剂成分产生了浓厚兴趣,联想到厕所清洁剂显酸性,其溶液pH______ 填“大于”或“小于”或“等于”
填“大于”或“小于”或“等于” ,请设计实验
,请设计实验 不再用测pH的方法
不再用测pH的方法 证明厕所清洁剂显酸性______。而且马桶中冲出的溶液显蓝色,对该现象同学们做出以下探究。
证明厕所清洁剂显酸性______。而且马桶中冲出的溶液显蓝色,对该现象同学们做出以下探究。
(提出问题)洁厕剂的主要成分是什么?
(猜想与假设)
猜想①:可能只含盐酸;
猜想②:可能只含硫酸铜;
猜想③:可能含有盐酸和硫酸铜。
其中猜想______遭到其他同学反对,原因是______。
(实验探究)为了验证其余两个猜想,同学们设计了以下实验进行探究:
实验操作 | 实验现象 | 实验结论 |
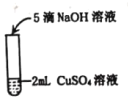
取少量洁厕剂加入适量的蒸馏水配成溶液。再取2mL配好的溶液于一支洁净试管中,并向其中逐滴加入足量氢氧化钠溶液 | __ | 猜想 |
写出上述实验中发生的化学方程式______ 写出一个即可
写出一个即可 。
。
某兴趣小组在实验室中探究氢氧化钠的性质,请你参与探究并填空
(实验过程与分析)
实验一 | 实验二 | 实验三 | |
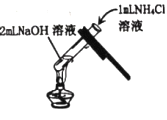
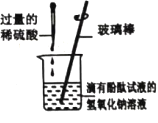
实验操作 |
|
|
|
实验现象 | _____ | _____ | 溶液由红色变为无色 |
实验分析 |
|
| 该中和反应实质是_____ |
实验结论 | _____ | _____ | 氢氧化钠能与硫酸发生反应 |


 不成立,猜想
不成立,猜想 成立
成立