题目内容
 (2010?南充)如图是某种胃药的部分标识.胃药中所含物质能中和胃液里过多的胃酸(主要是盐酸).某患者按标识上的服用方法服药,服药三天后病情好转.计算患者在三天内所服用的此胃药中:(计算结果保留一位小数)
(2010?南充)如图是某种胃药的部分标识.胃药中所含物质能中和胃液里过多的胃酸(主要是盐酸).某患者按标识上的服用方法服药,服药三天后病情好转.计算患者在三天内所服用的此胃药中:(计算结果保留一位小数)(1)所含氢氧化镁的质量为多少?
(2)理论上可中和胃酸中的HCl质量是多少?
分析:(1)首先可计算三天内患者共服用胃药2×3×3=18片,然后算出18片胃药含Mg(OH)2的质量.
(2)利用Mg(OH)2+2HCl═MgCl2+2H2O中Mg(OH)2与HCl的质量关系列式计算可得结果.
(2)利用Mg(OH)2+2HCl═MgCl2+2H2O中Mg(OH)2与HCl的质量关系列式计算可得结果.
解答:解:(1)服用三天共摄入体内氢氧化镁质量为 3×3×2×0.25g=4.5g
(2)设参加反应HCl质量为x
Mg(OH)2+2HCl=MgCl2+2H2O
58 73
4.5g x
=
解得 x≈5.7g
答:(1)所含氢氧化镁的质量为4.5g;
(2)理论上可中和胃酸中的HCl质量是5.7g;
(2)设参加反应HCl质量为x
Mg(OH)2+2HCl=MgCl2+2H2O
58 73
4.5g x
| 58 |
| 73 |
| 4.5g |
| x |
解得 x≈5.7g
答:(1)所含氢氧化镁的质量为4.5g;
(2)理论上可中和胃酸中的HCl质量是5.7g;
点评:本题主要考查学生运用化学方程式进行计算的能力.比较简单,关键是解题的步骤要规范.

练习册系列答案
相关题目
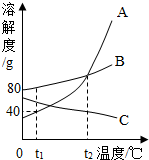 (2010?南充)如图所示是A、B、C三种固体物质的溶解度曲线.
(2010?南充)如图所示是A、B、C三种固体物质的溶解度曲线.