题目内容
【题目】某同学设计了如下图所示的装置,用于实验室制取CO2并对它的部分性质进行探究,请按要求答题。
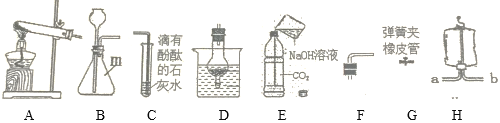
(1)仪器m的名称是______。
(2)在装置A、B中选______与H组合制取一袋二氧化碳,发生反应的化学方程式为________,验满的方法是________。若把G与_______组合成发生装置可控制反应的发生和停止,可通过_______(写出操作方法)可使反应停止。
(3)往图C中的试管通入CO2,当出现_______现象,表面石灰石的溶质刚好完全沉淀。
(4)向图E中的塑料软瓶中倒入一定量的NaOH溶液,迅速拧紧瓶盖,振荡,可观察到瓶子变瘪,但不能由此说明二氧化碳与氢氧化钠发生了反应,也可能是_______。
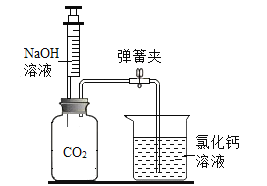
(5)为了验证氢氧化钠溶液与二氧化碳能发生反应,把上图中E装置改为如图装置。把注射器内的氢氧化钠溶液注入到装有二氧化碳的集气瓶中,打开弹簧夹,看到_____现象,写出产生此现象化学方程式_________、_________,证明二氧化碳与氢氧化钠溶液发生了化学反应。
【答案】锥形瓶 B CaCO3+2HCl═CaCl2+CO2↑+H2O 把燃着的木条放在b导管口,若木条熄灭,则证明已集满一袋二氧化碳 D 用弹簧夹夹紧橡胶管(或把干燥管取出) 酚酞溶液变成无色 二氧化碳与氢氧化钠溶液中的水发生反应(或CO2溶于水,或写反应方程式也给分) 烧杯中溶液倒流到集气瓶中,并出现白色沉淀 2NaOH+CO2═H2O+Na2CO3 Na2CO3+CaCl2=CaCO3↓+2NaCl
【解析】
(1)仪器m的名称是锥形瓶;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,反应物的状态是固体和液体,不需加热,属于固—液常温型,可用装置B与H组合制取一袋二氧化碳,大理石或石灰石的主要成分是碳酸钙,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;二氧化碳的密度大于空气,用H装置收集二氧化碳时,应从a导管通入,二氧化碳不能燃烧也不能支持燃烧,能使燃着的木条熄灭,验满的方法是:把燃着的木条放在b导管口,若木条熄灭,则证明已集满一袋二氧化碳;若把G与D组合成发生装置可控制反应的发生和停止,可通过用弹簧夹夹紧橡胶管(或把干燥管取出)可使固体与液体脱离接触,反应停止;
(3)往图C中的试管通入CO2,二氧化碳与氢氧化钙反应生成碳酸钙和水,溶液由碱性变成中性,当出现酚酞溶液变成无色现象,表明石灰水的溶质刚好完全沉淀;
(4)向图E中的塑料软瓶中倒入一定量的NaOH溶液,迅速拧紧瓶盖,振荡,可观察到瓶子变瘪,但不能由此说明二氧化碳与氢氧化钠发生了反应,也可能是:二氧化碳与氢氧化钠溶液中的水发生反应(或CO2溶于水);
(5)把图1中E装置改为图2装置。把注射器内的氢氧化钠溶液注入到装有二氧化碳的集气瓶中,打开弹簧夹,看到烧杯中溶液倒流到集气瓶中,并出现白色沉淀现象;因为二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,反应化学方程式分别为:2NaOH+CO2═H2O+Na2CO3;Na2CO3+CaCl2=CaCO3↓+2NaCl;

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】下列客观事实的解释中,正确的是![]()
![]()
选项 | 客观事实 | 解释 |
A | 品红在热水中扩散比在冷水中快 | 品红分子在不停地运动 |
B | 在压强不变时,气体的体积热胀冷缩 | 分子之间的间隔会随温度变化而变化 |
C | 用墨绘制的字能长久保存而不褪色 | 碳的化学性质不活泼 |
D | 金刚石和石墨物理性质不同 | 构成它们的碳原子结构不同 |
A. AB. BC. CD. D