题目内容
酸、碱、盐溶解性表是学习化学的重要工具.右表列出了“部分酸、碱、盐在20℃时的溶解性”.请回答:
| 阴离子 阳离子 | OH- | NO3- | Cl- | CO32- | SO42- |
| H+ | ---- | 溶、挥 | 溶、挥 | 溶、挥 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 不 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 不 | 溶 |
(2)从该表中找出下列物质(写化学式):一种没有挥发性的酸________;一种不溶于水的碱________;一种溶于水的钡盐________.
(3)写化学方程式:锌与表中的一种物质反应________.
解:(1)Ba(OH)2是三大强碱之一Na2SO4是钠盐,因此均可溶于水,故答案为:Na2SO4是可溶的(用表内物质,合理即可);
(2)由上表可知,酸有盐酸、硫酸和硝酸等,其中硫酸无挥发性;不溶于水的碱有氢氧化铜;不溶于水的盐很多,碳酸盐大部分不溶于水,如碳酸钡和碳酸钙,以及硫酸钡也不溶于水,故答案为:H2SO4;Cu(OH)2;BaCl2 (或Ba(NO3)2);
(3)锌可以和强酸反应,也可以和排在金属锌后面的金属的可溶性的盐反应,故答案为:Zn+H2SO4═ZnSO4+H2↑(用表内物质,合理即可).
分析:题考查的是酸碱盐的溶解性,给出表格,降低了难度,由上表可知,氢氧化钡能溶于水;我们学过的三大强酸有盐酸、硫酸和硝酸,弱酸有碳酸等;不溶于水的盐有很多,如碳酸钙、碳酸钡等大部分碳酸盐都不溶于水,硫酸钡不仅不溶于水,还不溶于三大强酸;金属与盐反应的条件是①前换后②盐是可溶于水的,金属锌能和强酸如硫酸和盐酸反应产生氢气和盐,书写化学方程式时要注意配平.
点评:本考点的综合性比较强,考查了酸碱盐的溶解性、复分解反应发生的条件、金属与盐溶液反应的条件和化学方程式的书写等,同学们要加强记忆,在理解的基础上要学会综合应用,达到学以致用的目标.
(2)由上表可知,酸有盐酸、硫酸和硝酸等,其中硫酸无挥发性;不溶于水的碱有氢氧化铜;不溶于水的盐很多,碳酸盐大部分不溶于水,如碳酸钡和碳酸钙,以及硫酸钡也不溶于水,故答案为:H2SO4;Cu(OH)2;BaCl2 (或Ba(NO3)2);
(3)锌可以和强酸反应,也可以和排在金属锌后面的金属的可溶性的盐反应,故答案为:Zn+H2SO4═ZnSO4+H2↑(用表内物质,合理即可).
分析:题考查的是酸碱盐的溶解性,给出表格,降低了难度,由上表可知,氢氧化钡能溶于水;我们学过的三大强酸有盐酸、硫酸和硝酸,弱酸有碳酸等;不溶于水的盐有很多,如碳酸钙、碳酸钡等大部分碳酸盐都不溶于水,硫酸钡不仅不溶于水,还不溶于三大强酸;金属与盐反应的条件是①前换后②盐是可溶于水的,金属锌能和强酸如硫酸和盐酸反应产生氢气和盐,书写化学方程式时要注意配平.
点评:本考点的综合性比较强,考查了酸碱盐的溶解性、复分解反应发生的条件、金属与盐溶液反应的条件和化学方程式的书写等,同学们要加强记忆,在理解的基础上要学会综合应用,达到学以致用的目标.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
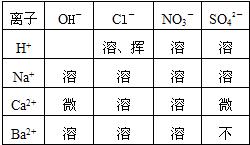 14、酸、碱、盐溶解性表是学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶解性.请利用此表完成以下任务:
14、酸、碱、盐溶解性表是学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶解性.请利用此表完成以下任务:
