题目内容
 (2005?卢湾区二模)氢氧化钙是一种碱,二氧化碳能与氢氧化钙溶液反应.氢氧化钾也是碱.那么,二氧化碳能否与氢氧化钾溶液也发生反应?
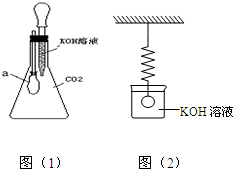
(2005?卢湾区二模)氢氧化钙是一种碱,二氧化碳能与氢氧化钙溶液反应.氢氧化钾也是碱.那么,二氧化碳能否与氢氧化钾溶液也发生反应?按照该思想方法,学生小组设计如右图(1)装置作探究:
锥形瓶内收满二氧化碳,滴管内盛有氢氧化钾溶液.挤压胶头滴管将氢氧化钾溶液滴入锥形瓶中.振荡后可见小气球a明显膨胀.
(1)反应原理:
CO2+2KOH=K2CO3+H2O
CO2+2KOH=K2CO3+H2O
.(2)试分析原因:
二氧化碳与氢氧化钾反应,使瓶内气体压强减小,大气压把气球鼓起
二氧化碳与氢氧化钾反应,使瓶内气体压强减小,大气压把气球鼓起
.(3)在以上实验后锥形瓶内的液体中滴加无色酚酞,显
红
红
色.接着以上学生实验,教师提供如图(2)所示装置:一只较灵敏的弹簧秤下,悬挂着一个实心的铜球,铜球浸没在盛有氢氧化钾溶液的烧杯中,此时弹簧秤的读数为M.教师请学生根据以上探究已有的结论推测:
(4)将烧杯敞开放置在空气中数天后,弹簧秤的读数将
小于M
小于M
.(假设溶液体积不变,且没有沉淀生成)(填“大于M”、“小于M”、“等于M”或“不能判断”)(5)因为:
烧杯敝开放置在空气中数天后,烧杯中氢氧化钾溶液吸收空气中二氧化碳而生成碳酸钾,使溶液质量增加,溶液体积不变而质量增加,根据ρ=
,可判断溶液密度增大,再根据F浮=ρ液V铜球g,可知铜球所受浮力增大,最后由弹簧秤的读数=G铜球-F浮,可得知此时弹簧秤的读数将小于M.
| m |
| v |
烧杯敝开放置在空气中数天后,烧杯中氢氧化钾溶液吸收空气中二氧化碳而生成碳酸钾,使溶液质量增加,溶液体积不变而质量增加,根据ρ=
,可判断溶液密度增大,再根据F浮=ρ液V铜球g,可知铜球所受浮力增大,最后由弹簧秤的读数=G铜球-F浮,可得知此时弹簧秤的读数将小于M.
.| m |
| v |
分析:(1)(2)二氧化碳与氢氧化钾反应生成碳酸钾和水,使瓶内气体压强减小,大气压把气球鼓起;
(3)二氧化碳与氢氧化钾反应生成碳酸钾,碳酸钾呈碱性,酚酞遇碱变红
(4)(5)烧杯敝开放置在空气中数天后,烧杯中氢氧化钡溶液吸收空气中二氧化碳而生成碳酸钡沉淀,使溶液质量减小,溶液体积不变而质量减小,则溶液密度减小,溶液密度的减小使铜球所受浮力减小,浮力的减小而使弹簧秤的读数增大.
(3)二氧化碳与氢氧化钾反应生成碳酸钾,碳酸钾呈碱性,酚酞遇碱变红
(4)(5)烧杯敝开放置在空气中数天后,烧杯中氢氧化钡溶液吸收空气中二氧化碳而生成碳酸钡沉淀,使溶液质量减小,溶液体积不变而质量减小,则溶液密度减小,溶液密度的减小使铜球所受浮力减小,浮力的减小而使弹簧秤的读数增大.
解答:解:(1)(2)二氧化碳与氢氧化钾反应生成碳酸钾和水,使瓶内气体压强减小,大气压把气球鼓起,故填:CO2+2KOH=K2CO3+H2O;二氧化碳与氢氧化钾反应,使瓶内气体压强减小,大气压把气球鼓起
(3)二氧化碳与氢氧化钾反应生成碳酸钾,碳酸钾呈碱性,酚酞遇碱变红,故填:红
(4)(5)烧杯敝开放置在空气中数天后,烧杯中氢氧化钾溶液吸收空气中二氧化碳而生成碳酸钾,使溶液质量增加,溶液体积不变而质量增加,根据ρ=
,可判断溶液密度增大,再根据F浮=ρ液V铜球g,可知铜球所受浮力增大,最后由弹簧秤的读数=G铜球-F浮,可得知此时弹簧秤的读数将小于M.
(3)二氧化碳与氢氧化钾反应生成碳酸钾,碳酸钾呈碱性,酚酞遇碱变红,故填:红
(4)(5)烧杯敝开放置在空气中数天后,烧杯中氢氧化钾溶液吸收空气中二氧化碳而生成碳酸钾,使溶液质量增加,溶液体积不变而质量增加,根据ρ=
| m |
| v |
点评:本题为跨学科的综合题,利用化学知识分析溶液质量的变化后,使用物理学知识对铜球所受浮力进行计算,综合使用各学科知识完成解答.

练习册系列答案
相关题目