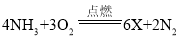题目内容
【题目】请根据下列实验装置图回答下列问题:
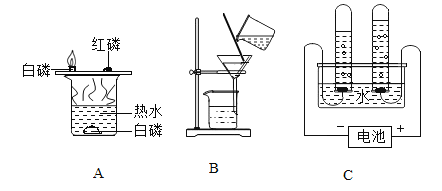
(1)实验A中热水的作用是提供热量和____________。
(2)B图所示操作的名称为____________,其中玻璃棒的作用是________。
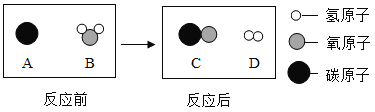
(3)C中电解水实验能得到的结论是:水是由_________组成的。
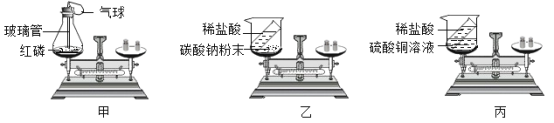
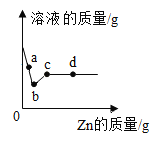
(4)某同学用上图中甲、乙、丙三个装置验证质量守恒定律,能得到正确结论的装置为____________(填序号)。由此可知验证质量守恒定律时,需注意的是_________(只回答一条即可)。试从微观角度分析化学反应前后质量守恒的原因是_____________。
【答案】隔绝空气 过滤 引流 氢元素和氧元素 甲 对有气体参与或生成的反应须使用密封装置(或试剂之间应发生化学反应) 反应前后原子的种类没有改变、数目没有增减,原子质量也没有改变
【解析】
(1)实验A中热水的作用是给铜片上的白磷提供热量和给水中的白磷隔绝氧气(或空气)。
(2)B图所示操作的名称为过滤,将不溶性固体和液体分开,其中玻璃棒的作用是引流,防止液体外洒。
(3)C中电解水实验,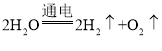 ,根据化学变化前后元素种类不变,能得到的结论是:水是由氢元素和氧元素组成的。
,根据化学变化前后元素种类不变,能得到的结论是:水是由氢元素和氧元素组成的。
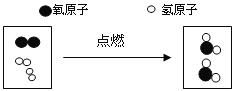
(4)用上图中甲、乙、丙三个装置验证质量守恒定律,甲可以发生化学反应: ,且在密闭容器中进行,故能验证质量守恒定律;乙能发生化学反应:
,且在密闭容器中进行,故能验证质量守恒定律;乙能发生化学反应:![]() ,该反应有气体生成,但装置不密闭,故不能验证质量守恒定律;丙装置不能发生化学反应,故不能验证质量守恒定律,故能得到正确结论的装置为甲。由此可知验证质量守恒定律时,需注意的是对有气体参与或生成的反应须使用密封装置或能发生化学反应。从微观角度分析化学反应前后质量守恒的原因是反应前后原子的种类没有改变、数目没有增减,原子质量也没有改变。
,该反应有气体生成,但装置不密闭,故不能验证质量守恒定律;丙装置不能发生化学反应,故不能验证质量守恒定律,故能得到正确结论的装置为甲。由此可知验证质量守恒定律时,需注意的是对有气体参与或生成的反应须使用密封装置或能发生化学反应。从微观角度分析化学反应前后质量守恒的原因是反应前后原子的种类没有改变、数目没有增减,原子质量也没有改变。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】某研究小组用下图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。

(提出猜想)
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,因为镁条可能会与空气中的其他成分发生反应
(进行实验)
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物还夹杂着极少量淡黄色的固体。 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5 |
(解释与结论)
(1)镁条与氧气反应的化学方程式为_____。
(2)步骤Ⅰ说明装置的气密性_____。
(3)步骤Ⅱ中,关闭止水夹的目的是_____。
(4)根据实验现象中的_____(写一个)可以推测猜想2成立。
(继续探究)经查阅资料得知氮化镁(Mg3N2)为淡黄色的固体。
(设计实验)设计实验证明镁与氮气发生了反应:_____。
(实验结论)镁条与氮气反应的化学方程式为:_____。
(反思与评价)通过上述探究活动,你对燃烧有什么新的认识?_____。
【题目】实验室用如图所示的装置制取二氧化碳,完全反应后,将锥形瓶中的剩余物过滤,探究得到的滤液中有哪些成分。
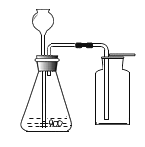
(提出猜想)猜想一:CaCl2 猜想二:CaCl2和_____(填化学式)
(实验探究)请你帮助他们完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量的滤液于试管中,再向试管中加入_____ | _____ | 猜想二正确 |