题目内容
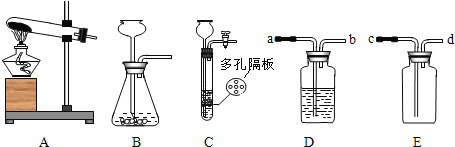
【题目】根据下图所示的实验回答问题:


(1)甲实验验证了氢氧化钙具有______________________________、________________________的化学性质。
(2)乙实验用pH试纸测定白醋的酸碱度时,先用蒸馏水润湿试纸,则测得结果与实际值相比________(填“偏大”“偏小”或“相等”)。
(3)丙实验中,稀硫酸必须用胶头滴管逐滴滴加,并用玻璃棒不断搅拌,这样做的目的是______________。写出稀硫酸与氢氧化钠反应的化学方程式:__________________________________。
【答案】 能与酚酞(指示剂)作用(或溶液显碱性) 能与稀盐酸反应 偏大 防止稀硫酸过量,使反应充分进行 2NaOH+H2SO4===Na2SO4+2H2O
【解析】(1)由甲实验可知,氢氧化钙溶液能使酚酞试液变成红色,加入稀盐酸后红色褪去,反映了氢氧化钙具有碱性和与酸反应的化学性质;(2)用蒸馏水润湿,再把白醋滴到试纸上,相当于稀释了白醋,则会使白醋的酸性变弱,由溶液的pH小于7时,呈酸性,且pH越小,酸性越强,故测得的结果与白醋实际的pH比较偏大;(3)丙实验中,稀硫酸必须用胶头滴管逐滴滴加,并用玻璃棒不断搅拌,这样做的目的是:防止稀硫酸过量,使反应充分快速.稀硫酸与氢氧化钠反应生成硫酸钠和水,反应的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O。

 名校课堂系列答案
名校课堂系列答案【题目】分析处理图表的信息是学习化学的一种重要方法。下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
(1)40 ℃时,氯化钠的溶解度为________g。
(2)碳酸钠的溶解度随温度的升高而________(填“增大”或“减小”)。在20 ℃时,在100 g的水中加入30 g碳酸钠,充分搅拌后得到的是________(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30 ℃,该溶液的溶质质量分数为________(计算结果精确到0.1%)。
(3)10 ℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是________________________________________________________________________。