题目内容
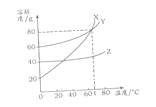
【题目】某兴趣小组用70g生锈铁钉与足量的一定溶质质量分数的稀盐酸反应。测得产生氢气的质量与稀盐酸的质量关系如图(假设铁钉中除表面含有氧化铁外,没有其他杂质)。
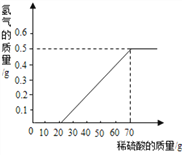
(1)当稀盐酸的质量为70g,产生的氢气的质量为______ g;
(2)用化学方程式说明当稀盐酸的质量为10g时,不产生氢气的原因:____;(用化学方程式说明)
(3)计算铁钉中单质铁的质量分数为_______________(写出计算过程)。
【答案】 0.5 Fe2O3+6HCl═2FeCl3+3H2O 20%
【解析】本题主要考查化学方程式进行计算和推断的能力,计算时要注意规范性和准确性。
(1)由图中信息可知,当稀盐酸的质量为70g,产生的氢气的质量为0.5g;
(2)当稀盐酸的质量为10g时,不产生氢气的原因是由于铁钉面存在氧化铁,稀盐酸先与氧化铁反应,因此最初稀盐酸加入时,不与铁反应生成氢气,而是先与氧化铁反应生成水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
(3)解:设铁钉中铁单质的质量为X,
Fe+2HCl═FeCl2+H2↑,
56 2
X 0.5g
![]() X═14g,
X═14g,
铁钉中单质铁的质量分数=![]() ×100%=20%,
×100%=20%,
答:铁钉中单质铁的质量分数为20%。

 53随堂测系列答案
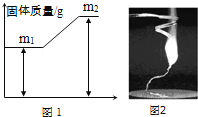
53随堂测系列答案【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验。
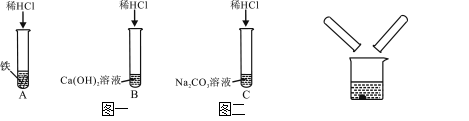
(1)A试管中的反应现象是 。
(2)C试管中反应的化学方程式是 。
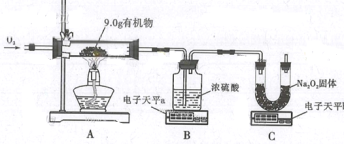
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、 HCl
你的猜想:有 。
【交流讨论】
你认为 同学的猜想一定不正确,理由是 。
【设计实验】请设计实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加 。 | _________________。 | 我的猜想成立 |
【反思与总结】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑 。