题目内容
金属元素R的最高价氧化物的化学式为RmOn,则R元素的最高化合价为 ;R元素(核电荷数小于18)原子最外电子层的电子数是 ;若RmOn的相对分子质量为Mr,则R元素的相对原子质量为. .
【答案】分析:根据在化合物中正负化合价代数和为零,结合RmOn的化学式进行解答;元素的正化合价数等于其原子的最外层电子数;根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
解答:解:氧元素显-2,设R元素的化合价是x,根据在化合物中正负化合价代数和为零,可知RmOn中R元素的化合价:mx+(-2)×n=0,则x=+ .
.
元素的正化合价数等于其原子的最外层电子数,故R元素(核电荷数小于18)原子最外电子层的电子数是 .
.
设R元素的相对原子质量为y,根据题意,RmOn的相对分子质量为Mr,则ym+16n=Mr,解得:y= .
.
故答案为:+ ;
;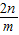 ;
; .
.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、有关化学式的计算等是正确解答本题的关键.
解答:解:氧元素显-2,设R元素的化合价是x,根据在化合物中正负化合价代数和为零,可知RmOn中R元素的化合价:mx+(-2)×n=0,则x=+
 .
.元素的正化合价数等于其原子的最外层电子数,故R元素(核电荷数小于18)原子最外电子层的电子数是
 .
.设R元素的相对原子质量为y,根据题意,RmOn的相对分子质量为Mr,则ym+16n=Mr,解得:y=
 .
.故答案为:+
 ;
;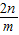 ;
; .
.点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、有关化学式的计算等是正确解答本题的关键.

练习册系列答案
相关题目