题目内容
(2010?青岛)某气体可能含有氢气、一氧化碳、二氧化碳、水蒸气和氯化氢中的一种或几种,为了确定其成分,将该气体依次进行如下实验(假设各步均完全反应):
①通过浓硫酸,浓硫酸质量增加;②通过澄清石灰水,石灰水不变浑浊;③先通过浓硫酸,再通过灼热的氧化铜,固体由黑色变成红色;④通过无水硫酸铜,固体不变色(无水硫酸铜具有遇水变蓝的性质);⑤通过澄清石灰水,石灰水变浑浊.
请根据上述实验现象推断,并用化学式填空:该气体中一定有
①通过浓硫酸,浓硫酸质量增加;②通过澄清石灰水,石灰水不变浑浊;③先通过浓硫酸,再通过灼热的氧化铜,固体由黑色变成红色;④通过无水硫酸铜,固体不变色(无水硫酸铜具有遇水变蓝的性质);⑤通过澄清石灰水,石灰水变浑浊.
请根据上述实验现象推断,并用化学式填空:该气体中一定有
H2O CO
H2O CO
,一定没有H2
H2
,无法确定的是CO2HCl
CO2HCl
.分析:由题意可知,按照实验步骤依次进行实验.①浓硫酸具有吸水性,浓硫酸质量增加,说明气体中有水蒸气.②通过澄清石灰水,石灰水不变浑浊.我们知道二氧化碳能使石灰水变浑浊,但是若有氯化氢气体存在时,氯化氢与石灰水发生中和反应,二氧化碳失去与石灰水反应的机会.又因氯化氢气体不能确定,故不能确定二氧化碳是否存在.有该部能得出的结论是:没有氯化氢,一定没有二氧化碳;若有氯化氢,不一定有二氧化碳.③先通过浓硫酸,再通过灼热的氧化铜,固体由黑色变成红色,说明一定含有具有还原性的气体,在所给气体中氢气和一氧化碳都具有还原性.故该部不能确定.④通过无水硫酸铜,固体不变色(无水硫酸铜具有遇水变蓝的性质),说明气体夺氧后没有水生成,故气体中不含有氢气,那就一定含有一氧化碳.⑤通过澄清石灰水,石灰水变浑浊,进一步确定,气体夺氧后生成了二氧化碳,说明原气体中一定含有一氧化碳.
解答:解:由①得出结论是一定有水蒸气;由②得出结论是若没有氯化氢,就一定没有二氧化碳;若有氯化氢,还不一定有二氧化碳,故原气体中的二氧化碳和氯化氢都不能确定;由③得出的结论是一定有还原性气体;由④得出的结论是一定没有氢气,一定有一氧化碳;⑤进一步确定含有一氧化碳.
故答案为:H2O CO; H2; CO2HCl
故答案为:H2O CO; H2; CO2HCl
点评:该题是实验推断题,在熟练掌握各气体性质的基础上,主要考查分析推理能力.关键是严谨全面.

练习册系列答案
相关题目
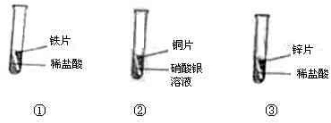 (2010?青岛)某化学兴趣小组为探究铁、铜、锌、银的金属活动性顺序,设计了下图所示的三个实验(其中就是均已打磨,且形状、大小相同;所用盐酸的溶质质量分数、用量也相同).下列判断中,错误的是( )
(2010?青岛)某化学兴趣小组为探究铁、铜、锌、银的金属活动性顺序,设计了下图所示的三个实验(其中就是均已打磨,且形状、大小相同;所用盐酸的溶质质量分数、用量也相同).下列判断中,错误的是( )