题目内容
【题目】碳与氧化铜恰好完全反应,有关量的变化见右下图,分析正确的是
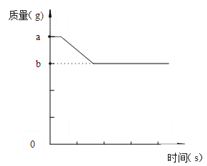
A. (a-b)表示反应消耗的碳的质量
B. (a-b)表示反应前后固体中氧元素的质量
C. b表示生成的铜的质量
D. b表示生成的二氧化碳的质量
【答案】C
【解析】
根据木炭还原氧化铜的反应原理书写方程式,根据方程式并结合图象进行分析,作出正确的判断。
解:木炭还原氧化铜的化学反应方程式为:C+2CuO![]() 2Cu+CO2↑,由图象可知:随着反应的进行,物质的质量逐渐减小,恰好完全反应后不再发生变化,则纵坐标表示的是固体的质量;
2Cu+CO2↑,由图象可知:随着反应的进行,物质的质量逐渐减小,恰好完全反应后不再发生变化,则纵坐标表示的是固体的质量;
A、由反应方程式知,反应前固体是碳与氧化铜,反应后固体为铜,依据质量守恒定律可知:a﹣b,固体质量的减少是生成的二氧化碳的质量,故错误;
B、由A分析可知,减少的应该是二氧化碳的质量,故错误;
C、反应生成的固体是铜,则b表示的是生成的铜的质量,正确;
D、b是生成的铜的质量,不是二氧化碳的质量,故错误;
故选:C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目