题目内容
通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中的内容,并回答相应的问题.
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的
(2)由中间两行内容对照可得出的规律是:通过元素或原子团的
(3)根据表格中所给内容,请你再写出一种类似于MgCl2或Na2SO4的化合物的化学式:
(4)根据硫酸亚铁的化学式FeSO4可推出该物质所含阳离子的符号为
| 常见的几种离子 | H+ Na+ Mg2+ OH- Cl- SO
| ||||||||||||||||
| 对应元素及原子团在 化合物中的化合价 |
| ||||||||||||||||
| 所能写出化合物的化学式 | HCl、 H2SO4 |
NaOH、 Mg(OH))2 |
MgCl2、 Na2SO4 | ||||||||||||||
| 写出相对应的名称 | 盐酸、 硫酸 |
氢氧化钠 氢氧化钠 、氢氧化镁 氢氧化镁 |
氯化镁 氯化镁 、硫酸钠 硫酸钠 | ||||||||||||||
电荷
电荷
数相等.(2)由中间两行内容对照可得出的规律是:通过元素或原子团的
化合价
化合价
可以确定相应的化合物的化学式.(3)根据表格中所给内容,请你再写出一种类似于MgCl2或Na2SO4的化合物的化学式:
MgSO4或NaCl
MgSO4或NaCl
.(4)根据硫酸亚铁的化学式FeSO4可推出该物质所含阳离子的符号为
Fe2+
Fe2+
.分析:根据已有的知识进行分析,离子所带的电荷数与化合价数值相等;根据化合价可以确定物质的化学式;根据化学式可以知道其中所含有的离子,据此解答.
解答:解:碱命名时读作氢氧化某,故NaOH读作氢氧化钠,Mg(OH))2读作氢氧化镁;由两种元素组成的物质,从右向左读作某化某,故MgCl2读作氯化镁,含氧酸盐命名时读作某酸某,故Na2SO4读作硫酸钠,故填:
(1)根据前前两行内容对照可以看出,元素或原子团的化合价数值往往与相应离子所带的电荷数相等,故填:电荷;
(2)通过元素或原子团的化合价可以确定相应的化合物的化学式,故填:化合价;
(3)MgCl2和Na2SO4属于盐,故可以写出硫酸镁和氯化钠的化学式,故填:MgSO4或NaCl;
(4)在FeSO4中,硫酸根的根价为-2,故铁元素的化合价为+2,故阳离子所带的电荷数为2个单位的正电荷,故填:Fe2+.
| 见的几种离子 | H+ Na+ Mg2+ OH- Cl- SO
| ||||||||||||||||
| 对应元素及原子团在 化合物中的化合价 |
| ||||||||||||||||
| 所能写出化合物的化学式 | HCl、 H2SO4 |
NaOH、 Mg(OH))2 |
MgCl2、 Na2SO4 | ||||||||||||||
| 写出相对应的名称 | 盐酸、 硫酸 |
氢氧化钠、 氢氧化镁 |
氯化镁、硫酸钠 | ||||||||||||||
(2)通过元素或原子团的化合价可以确定相应的化合物的化学式,故填:化合价;
(3)MgCl2和Na2SO4属于盐,故可以写出硫酸镁和氯化钠的化学式,故填:MgSO4或NaCl;
(4)在FeSO4中,硫酸根的根价为-2,故铁元素的化合价为+2,故阳离子所带的电荷数为2个单位的正电荷,故填:Fe2+.
点评:本题考查了化学用语,完成此题,可以依据已有的知识进行.记住元素符号周围数字表示的意义.

练习册系列答案
相关题目
通过对已学知识的对比和归纳,可以得出一些十分有趣的规律.这些规律可以帮助我们掌握学习化学的方法.请你仔细阅读表中的内容,并回答相应的问题.
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 数相等:
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式.
(3)利用表格中所给内容,请你再写出一种全都由非金属元素组成且含有原子团的化合物的化学式 .
(4)请你写出由H+、Na+、SO42-三种离子组成的物质的化学式 .
| 常见的几种离子 | H+ Na- Mg2+ OH- Cl- SO42 | ||
| 对应元素及原子团在化合物中的化合价 |  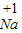     | ||
| 所能形成化合物的化学式 | 含有氢离子的化合物举例 | 含有氢氧根离子的化合物举例 | 其他化合物举例 |
| HCl、H2SO4 | NaOH、Mg(OH)2 | MgCl2、Na2SO4 | |
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式.
(3)利用表格中所给内容,请你再写出一种全都由非金属元素组成且含有原子团的化合物的化学式 .
(4)请你写出由H+、Na+、SO42-三种离子组成的物质的化学式 .
