题目内容
(7分)人类社会的发展离不开常见金属和金属材料,用我们学到的化学知识和方法能分析和解释许多现象。
(1)下列生活用品,主要利用金属具有良好导热性的是:___ ____。
A.铸铁炊具 B.金属细丝 C.铜制电缆 D.铁锤
(2)常见的三种金属被发现、使用的先后顺序依次为:铜、铁、铝。金属大规模被使用的先后顺序跟下列___ ____(填序号)选项关系最大。
①地壳中金属元素的含量 ②金属的导电性 ③金属活动性
(3)工业上用赤铁矿(主要成份为氧化铁)炼铁的化学反应方程式为___ ____。世界上每年有近四分之一的钢铁被锈蚀,为了保护金属资源我们必须学会防锈,下列介绍的实例只利用隔绝氧气来达到防锈的是:___ ____。



A、菜刀用完后擦拭干净存放
B、自行车三角架涂漆
C、夏季停暖后暖气片内注满水防止内部生锈
D、用不锈钢制造炊具
(4)工业生产中,切割铁板时用硫酸铜溶液在铁板上画线可留下红色的印迹。有关反应的化学方程式为___ ____。
(5)铁粉常用作双吸剂,将一包部分变质的双吸剂放入过量稀盐酸中,充分反应后所得溶液中的溶质可能是___ ____。(友情提示:在溶液中可发生Fe+2FeCl3=3FeCl2反应)
(1) A (2) ③
(3)Fe2O3+3CO高温2Fe+3CO2 C 。
(4)Fe+CuSO4=Cu+FeSO4。
(5)①FeCl2、HCl②FeCl2、FeCl3和HCl。
解析试题分析:(1)根据金属的物理性质分析。
A.铸铁炊具主要利用金属具有良好的导热性;
B.金属细丝主要利用金属具有良好的延展性;
C.铜制电缆主要利用金属具有良好的导电性;
D.铁锤主要利用金属硬度较大的性质。故选A
(2)金属的活动性越强,就越难冶炼,故大规模被使用也就越晚,所以金属大规模被使用的先后顺序跟金属活动性有关,故选③。
(3)工业上一般用一氧化碳还原氧化铁,生成铁和二氧化碳,故反应的化学方程式为Fe2O3+3CO高温 2Fe+3CO2;铁在潮湿的空气中易生锈,即铁的生锈是铁与氧气和水共同作用的结果,因此防锈一般要隔绝氧气和水,但夏天停暖后气片内注满水防止内部生锈,只是隔绝氧气防锈,故选C。
(4)铁可与硫酸铜溶液发生置换反应,生成红色的铜,从而留下红色的印迹,故化学反应的方程式为Fe+CuSO4═Cu+FeSO4。
(5)双吸剂变质即有部分铁生锈,生成氧化铁,故将其投入过量的盐酸中,发生的化学反应有Fe+2HCl=FeCl2+H2↑、Fe2O3+6HCl=2FeCl3+3H2O,再结合题干提供的反应Fe+2FeCl3=3FeCl2可知,溶液中一定有生成的氯化亚铁及剩余的盐酸;当铁的量较多时,会将生成的FeCl3完全反应,当铁的量较少时,就不会将生成的FeCl3完全反应,故氯化铁可能存在。
考点:常见金属的物理性质,金属活动性的应用,金属的冶炼,金属锈蚀的条件及其防护,金属及金属氧化物的化学性质
点评:本题主要是让我们结合生活常识和所学化学知识,探究日常生活中常见金属及其制品的物理和化学性质,涉及知识面较广,除了要求学生要具有扎实的基础知识之外,还要有较强的分析、解决问题的能力。

(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属
(2)西气东输,将改变我市居民的气体燃料结构.下表是几种气体燃料的价格和热值:
| 燃烧物 | 煤气 | 液化石油气 | 天然气 |
| 价格 | 1.4元/千克 | 6.0元/千克 | 1.8元/千克 |
| 热值 | 1.56×104kJ/kg | 4.5×104kJ/kg | 3.9×104kJ/kg |
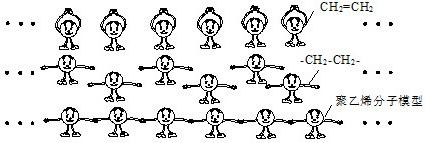
(3)化石燃料不仅是优质的能量资源,还是宝贵的化工资源.聚乙烯是一种最常用的塑料,它是以石油裂解气体乙烯(CH2=CH2)为原料,经许多乙烯分子打开双键(-CH2-CH2-)连在一起,聚合成大分子而形成的.下图是聚乙烯分子形成过程的示意图,卡通画中单个小人代表一个乙烯分子.聚乙烯其中的部分结构可表示为:…
(4)开发和利用清洁高效而又用之不竭的新能源,是21世纪人类面临的重要课题.
①2006年1月起,我省苏北四市推广使用乙醇汽油.乙醇可利用农作物发酵制得,农作物在催化剂作用下转化为葡萄糖(C6H12O6),然后葡萄糖在酒化酶的作用下转化为乙醇和二氧化碳,写出葡萄糖转化为乙醇的化学方程式
②氢气是一种未来理想的能源.现通过生物法制得的氢气中混有CO2、O2和水蒸气等(氢气的体积分数通常为60%~90%),为了得到纯净的氢气,将混合气体依次通过NaOH溶液、灼热的Cu丝和干燥装置.该除杂方案是否正确?

