题目内容
【题目】人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
(1)西汉时期中国古老的冶铜方法是“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,写出反应的化学方程式 .
(2)铁锅、铝锅是生活中常用的炊具,如图1是铁锅的示意图. 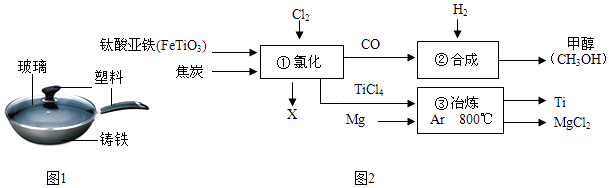
①铁锅含有的有机合成材料是 . (填写名称).
②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是 .
③铜也易生锈,铜锈的主要成分是碱式碳酸铜(Cu(OH)2CO3),是铜与空气中的氧气、水和共同作用的结果.
(3)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、航天飞机、船舶等,如图2为某化工企业生产钛流程示意图: 请回答下列问题:
①FeTiO3中钛元素的化合价为;
②中化学方程式为2FeTiO3+6C+7Cl2 ![]() 2C+2TiCl4+6CO2 , 则X为(填化学式).
2C+2TiCl4+6CO2 , 则X为(填化学式).
③中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是 .
④中氩气的作用是 , 该步反应的化学方程式为 .
【答案】
(1)Fe+CuSO4=FeSO4+Cu
(2)塑料;隔绝氧气;二氧化碳
(3)+4;FeCl3;化合反应;保护气;2Mg+TiCl4 ![]() Ti+2MgCl2
Ti+2MgCl2
【解析】解:(1)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;(2)①铁锅含有的有机合成材料是:塑料;②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是:隔绝氧气;③铜生锈是铜与空气中的氧气、水和二氧化碳共同作用的结果;(3)①在FeTiO3中,铁元素显+2价,氧元素显示﹣2价, 设钛元素的化合价为x,+2+x+(﹣2)×3=0,x=+4,
所以钛元素的化合价为+4价;②化学反应前后,元素质量不变,反应物中2个铁原子,2个钛原子,6个氧原子,6个碳原子,14个氯离子,生成物中有2个钛原子,8个氯原子,6个碳原子,6个氧原子,所以X是FeCl3;③CO和H2以化学计量数1:2恰好完全反应生成了CH3OH,所以该反应的基本反应类型是化合反应;④稀有气体的化学性质稳定,可以作保护气,镁和四氯化钛在800℃的条件下生成钛和氯化镁,化学方程式为:2Mg+TiCl4 ![]() Ti+2MgCl2 .
Ti+2MgCl2 .
所以答案是:(1)Fe+CuSO4=FeSO4+Cu;(2)①塑料;②隔绝氧气;③二氧化碳;(3)①+4;②FeCl3;③化合反应;④保护气,2Mg+TiCl4 ![]() Ti+2MgCl2 .
Ti+2MgCl2 .
【考点精析】掌握金属材料的选择依据和质量守恒定律及其应用是解答本题的根本,需要知道黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏.

