题目内容
根据图1和图2回答问题:
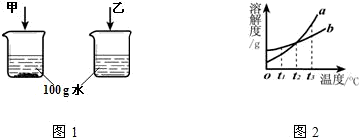
(1)甲、乙溶液中的溶剂是________.
(2)在t1℃时,等质量的甲、乙两种固体物质在水中的溶解现象如图1所示,要使剩余的甲固体继续溶解可采用的方法是________.
(3)图2中a、b分别表示上述两种物质的溶解度曲线,在________℃时,这两种物质的溶解度相等;b表示的是________物质(填“甲”或“乙”)的溶解度曲线.
(4)如图所示,小烧杯中盛放的是t2℃时所得的甲物质的饱和溶液.若将适量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是________(填字母).
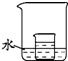
A.冰 B.浓硫酸 C.硝酸铵
D.干冰 E.氢氧化钠 F.氧化钙.
解:(1)甲、易溶液中,溶解物质的是水,所以溶剂是水.
故答案为:水;
(2)由图1可知,在t1℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此b代表的是乙,a代表的是甲,由于甲的溶解度随温度的升高而明显增大,因此可以通过加水或升高温度的方法使剩余的甲固体继续溶解.
故答案为:加水(或升温);
(3)由于在t2℃时,两物质的溶解度曲线交于一点,即两物质的溶解度相等;由图1可知,在t1℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此b代表的是乙,a代表的是甲.
故答案为:t2;乙;
(4)因为甲的溶解度随温度的升高而增大,所以只要能使小烧杯中的温度降低的就可以使固体析出.即只要加到大烧杯中的物质能够吸热即可.
A、冰融于水要吸热; B、浓硫酸溶于水要放热; C、硝酸铵溶于水要吸热; D、干冰气化要吸热; E、氢氧化钠溶于水要放热;F、氧化钙溶于水要放热.
故答案为:ACD
分析:(1)观察图示并根据溶剂的定义判断;
(2)观察图示可知,甲、乙两种物质的溶解度随温度的上升而增大,从而确定剩余的甲固体继续溶解的方法;
(3)观察图2ab交于一点时的温度就是两种物质的溶解度相等的温度;根据图1中甲、乙物质的溶解度判断;
(4)观察表中数据可知,甲的溶解度随温度的升高而增大.因为t2℃的溶液是甲的饱和溶液,所以只要能使饱和溶液温度降低的就能让小烧杯中有固体析出.
点评:根据物质实际的溶解现象与溶解度曲线的特点相结合,可以确定物质的溶解度曲线.同学们只要牢牢把握住溶解度的概念即可.溶解度:某温度下,100g溶剂中最多溶解的溶质的质量.要注意一下几点:谈论溶解度必须指明温度,没有指明温度的溶解度是没有意义的;溶解度指的是100g水中最多溶解的溶质的质量.
故答案为:水;
(2)由图1可知,在t1℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此b代表的是乙,a代表的是甲,由于甲的溶解度随温度的升高而明显增大,因此可以通过加水或升高温度的方法使剩余的甲固体继续溶解.
故答案为:加水(或升温);
(3)由于在t2℃时,两物质的溶解度曲线交于一点,即两物质的溶解度相等;由图1可知,在t1℃时,100克水中溶解的乙物质多,即乙的溶解度大,因此b代表的是乙,a代表的是甲.
故答案为:t2;乙;
(4)因为甲的溶解度随温度的升高而增大,所以只要能使小烧杯中的温度降低的就可以使固体析出.即只要加到大烧杯中的物质能够吸热即可.
A、冰融于水要吸热; B、浓硫酸溶于水要放热; C、硝酸铵溶于水要吸热; D、干冰气化要吸热; E、氢氧化钠溶于水要放热;F、氧化钙溶于水要放热.
故答案为:ACD
分析:(1)观察图示并根据溶剂的定义判断;
(2)观察图示可知,甲、乙两种物质的溶解度随温度的上升而增大,从而确定剩余的甲固体继续溶解的方法;
(3)观察图2ab交于一点时的温度就是两种物质的溶解度相等的温度;根据图1中甲、乙物质的溶解度判断;
(4)观察表中数据可知,甲的溶解度随温度的升高而增大.因为t2℃的溶液是甲的饱和溶液,所以只要能使饱和溶液温度降低的就能让小烧杯中有固体析出.
点评:根据物质实际的溶解现象与溶解度曲线的特点相结合,可以确定物质的溶解度曲线.同学们只要牢牢把握住溶解度的概念即可.溶解度:某温度下,100g溶剂中最多溶解的溶质的质量.要注意一下几点:谈论溶解度必须指明温度,没有指明温度的溶解度是没有意义的;溶解度指的是100g水中最多溶解的溶质的质量.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目