题目内容
在两个烧杯里各放等质量等质量分数足量稀盐酸.向其中一个烧杯中放入5.6g氧化钙,另一个烧杯里放入一定量的碳酸钙,充分反应后,烧杯中溶液总质量相等,则另一个烧杯中加入碳酸钙的质量是
- A.5.6g
- B.10 g
- C.8g
- D.无法判断
B
分析:由化学方程式可以看出,碳酸钙比氧化钙多出的质量,生成二氧化碳逸出,故若使天平继续保持平衡,只要消耗盐酸的质量相等即可.
①根据氧化钙与盐酸反应的化学方程式,列出比例式,就可计算出参与反应的HCl的质量;
②如果天平继续保持平衡,碳酸钙消耗的盐酸质量与氧化钙消耗盐酸的质量相等,根据碳酸钙与盐酸反应的化学方程式,列出比例式,就可计算出应向右盘加碳酸钙的质量.
解答:①设氧化钙参与反应的HCl的质量为x,
2HCl+CaO=CaCl2+H2O
73 56
x 5.6g

解之得:x=7.3g;
②设加碳酸钙的质量为y,
2HCl+CaCO3=CaCl2+H2O+CO2↑
73 100
7.3g y
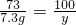
解之得:y=10g.
故选B.
点评:本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
分析:由化学方程式可以看出,碳酸钙比氧化钙多出的质量,生成二氧化碳逸出,故若使天平继续保持平衡,只要消耗盐酸的质量相等即可.
①根据氧化钙与盐酸反应的化学方程式,列出比例式,就可计算出参与反应的HCl的质量;
②如果天平继续保持平衡,碳酸钙消耗的盐酸质量与氧化钙消耗盐酸的质量相等,根据碳酸钙与盐酸反应的化学方程式,列出比例式,就可计算出应向右盘加碳酸钙的质量.
解答:①设氧化钙参与反应的HCl的质量为x,
2HCl+CaO=CaCl2+H2O
73 56
x 5.6g

解之得:x=7.3g;
②设加碳酸钙的质量为y,
2HCl+CaCO3=CaCl2+H2O+CO2↑
73 100
7.3g y
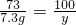
解之得:y=10g.
故选B.
点评:本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目