题目内容
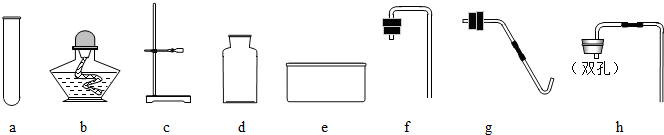
实验室用加热高锰酸钾制氧气,现有15.8g高锰酸钾,最多能制得氧气的质量为多少?
解:设最多能制得氧气的质量为x克
2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
316 32
15.8g x
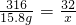
解得:x=1.6g
答:最多能制得氧气的质量为1.6g.
分析:根据高锰酸钾受热分解的化学方程式,可得知反应中高锰酸钾与氧气的质量关系,再由生成高锰酸钾的质量即可计算生成的氧气的质量.
点评:本题为根据化学方程式计算类问题中的基础计算,完整的计算步骤、规律的书写格式是解答此类问题时需要留意的地方.
2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑316 32
15.8g x
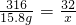
解得:x=1.6g
答:最多能制得氧气的质量为1.6g.
分析:根据高锰酸钾受热分解的化学方程式,可得知反应中高锰酸钾与氧气的质量关系,再由生成高锰酸钾的质量即可计算生成的氧气的质量.
点评:本题为根据化学方程式计算类问题中的基础计算,完整的计算步骤、规律的书写格式是解答此类问题时需要留意的地方.

练习册系列答案
相关题目