题目内容
【题目】下图是实验室制取氧气可能用到的装置。
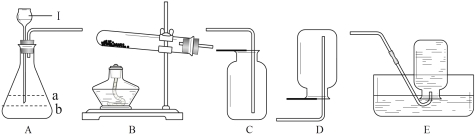
(1)写出编号仪器的名称:Ⅰ 。
(2)制取氧气时A中锥形瓶内应先加入的物质是 ,其作用是 。锥形瓶内液体应加至 (填“a”或“b”)处。写出以A为发生装置制取氧气的化学方程式: 。
(3)收集氧气选用的装置是上图E或 ,选择E的理由是 。
(4)用氯酸钾和二氧化锰的混合物制取氧气,实验中固体的质量变化如下:

①生成氧气的质量是 g,其物质的量为 mol。
②求参加反应的氯酸钾的物质的量。(根据化学方程式列式计算)
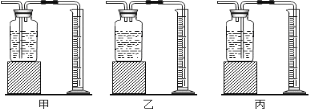
(5)为测定氯酸钾分解生成氧气的体积,应选用下图装置 (填编号)。
【答案】(1) 长颈漏斗(2)二氧化锰 加快反应速度 a 2H2O2![]() 2H2O+O2↑(3)C 氧气不(微)溶于水 (4) 4.8 0.15 0.2mol (5)丙
2H2O+O2↑(3)C 氧气不(微)溶于水 (4) 4.8 0.15 0.2mol (5)丙
【解析】
试题分析:(1)图中仪器I的名称为长颈漏斗;(2)制取氧气时A中锥形瓶内应先加入的物质是二氧化锰,作用为加快反应速率(或催化作用)为防止长颈漏斗漏气,锥形瓶中的液体应该加到超过长颈漏斗的下端,故选择a,处;发生装置制取氧气的化学方程式2H2O2![]() 2H2O+O2↑;(3)因为氧气不易溶于水,密度比空气的大,故可采用向上排空气法和排水集气法收集,故选择E或C都行;(4)①根据质量守恒定律可知,反应后质量减少即为生成的氧气的质量:(15g+5g-15.2g=4.8g;其物质的量为:4.8g÷32g/mol=0.15mol
2H2O+O2↑;(3)因为氧气不易溶于水,密度比空气的大,故可采用向上排空气法和排水集气法收集,故选择E或C都行;(4)①根据质量守恒定律可知,反应后质量减少即为生成的氧气的质量:(15g+5g-15.2g=4.8g;其物质的量为:4.8g÷32g/mol=0.15mol
②设:原混合物中氯酸钾的物质的量X mol
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
2 3
X 0.15 mol
![]() =
=![]() X=0.2(mol)
X=0.2(mol)
答原混合物中氯酸钾的物质的量0.2mol
(5)为测定氯酸钾分解生成氧气的体积,应选用下图丙装置,短管进入长管把水压入量筒中测定体积。

【题目】除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是
选项 | 待提纯的物质 | 选用的试剂 | 操作的方法 |
A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
B | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
C | Cu(CuO) | 稀硫酸 | 溶解、过滤、洗涤、干燥 |
D | CO2(CO) | 氧气 | 点燃 |