题目内容
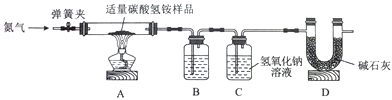
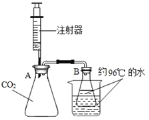
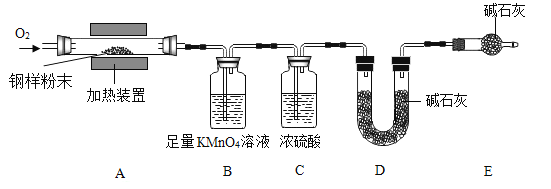
【题目】为测定钢铁中的含碳量,设计如下装置,钢铁样品在装置A中煅烧时,气体产物只有CO2和SO2。
(1)钢样处理成粉末的主要目的是______。钢样中的Fe3C煅烧时的化学方程式为Fe3C+3O2![]() ______+CO2。
______+CO2。
(2)实验室用KClO3和MnO2制备O2的化学方程式为______,MnO2中Mn的化合价为______。
(3)装置 B的作用是______,装置 B中的现象是______。
(4)装置C的作用是______。若无装置C,则测定结果______(填“偏大”“无影响”或“偏小”)。
(5)装置D的作用为______;装置E的作用为______。
(6)钢样中加入某物质可降低煅烧温度,为不影响测定结果,该物质在组成上需满足的条件是______。
【答案】增大反应物接触面积,使反应更充分 Fe3O4 ![]() +4价 除去CO2中的SO2 高锰酸钾溶液褪色 吸收CO2中的水蒸气 偏大 吸收CO2,测定产生的CO2质量 防止空气的CO2和H2O进入D装置 不能含有碳元素
+4价 除去CO2中的SO2 高锰酸钾溶液褪色 吸收CO2中的水蒸气 偏大 吸收CO2,测定产生的CO2质量 防止空气的CO2和H2O进入D装置 不能含有碳元素
【解析】
(1)钢样处理成粉末的主要目的是增大反应物接触面积,使反应更充分,根据化学反应前后原子个数守恒,反应的化学方程式Fe3C+3O2![]() Fe3O4+CO2;
Fe3O4+CO2;
(2)实验室用氯酸钾制备氧气的化学方程式为![]() ;根据化合物中各元素的正负化合价代数和为零,可计算出锰的化合价为+4价;
;根据化合物中各元素的正负化合价代数和为零,可计算出锰的化合价为+4价;
(3)为准确测定含碳量,要排除二氧化硫的干扰,所以装置 B的作用是除去CO2中的SO2,可以观察到高锰酸钾溶液褪色;
(4)为准确测定含碳量,要排除水蒸气的干扰,所以装置 C的作用是吸收CO2中的水蒸气,若无该装置,最后吸收的二氧化碳会混有水蒸气,使测定结果亦偏大;
(5)装置D的作用为吸收CO2,测定产生CO2的质量;装置E的作用为防止空气的CO2和H2O进入D装置;
(6)钢样中加入某物质可降低煅烧温度,为不影响测定结果,该物质在组成上需满足的条件是不能含有碳元素。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
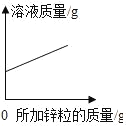
红果子三级测试卷系列答案【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
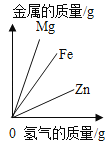
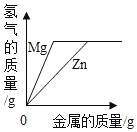
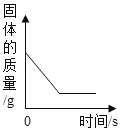
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D
【题目】“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术,他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜 想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如图所示
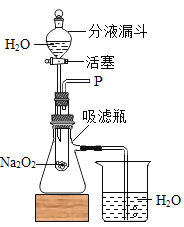
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开上图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是________;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______________。
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能。为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验:
实验步骤 | 实验现象 | 实验结论 |
_________ | _________ | 生成物中没有 |
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞溶液,发现试管中的溶液变成红色,说明反应后所得的溶液呈________性。
[表达]小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为_________________。