题目内容
【题目】某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三(2)班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)复习常见金属活动顺序表,在下表空格中分别填入对应的元素符号。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Pt Au
![]() 金属活动性由强到弱
金属活动性由强到弱
(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题:

①废水在加入金属X前需进行过滤,目的是将其中 性杂质除去。进行过滤的操作所需的仪器有: (请从下图中选择合适仪器,并用仪器序号填写)。
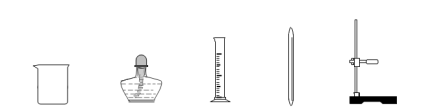
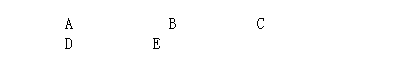
②金属X是 ,其加入废水后发生反应的化学方程式为 ;
溶液Y是 ,利用其除去铜中杂质,有关反应的化学方程式为
【答案】(1)Ag
(2 )①不溶性杂质 ADE
②Fe Fe+CuSO4=Cu+ Fe CuSO4
【解析】缺少漏斗,所以(2)中不能选E
分析:熟练记忆金属活动性顺序表是解决此类问题的基础.在解决本题的第二部分内容时,要充分考虑到最终需要通过冷却滤液结晶回收滤液中的硫酸亚铁,因此,操作过程中不能产生新的杂质.
解答:解:①根据金属活动性顺序表的记忆进行再现.故答:Ag;过滤操作使用的玻璃仪器有:烧杯、漏斗和玻璃棒.故答:AD;
②根据题意,应选择金属铁与硫酸铜反应,置换出金属铜同时生成硫酸亚铁使接下来回收的硫酸亚铁晶体更纯净.故答:铁,Fe+CuSO4=FeSO4+Cu;
为除去混在铜中的铁并生成硫酸亚铁,应选择硫酸与铁反应.故答:稀硫酸;Fe+H2SO4=FeSO4+H2↑.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目