题目内容
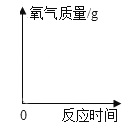
【题目】向一定质量的MgSO4溶液中先后滴加100克Ba(OH)2、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图。下列说法正确的是
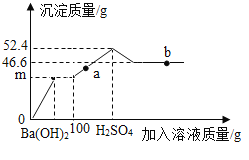
A.a点对应的溶液pH<7
B.b点溶液中的溶质只有1种
C.m=23.3
D.Ba(OH)2溶液溶质质量分数一定等于34.2%
【答案】D
【解析】
A、a点处于加入硫酸产生的沉淀不断增加的过程中,说明对应的溶液中含有氢氧化钡,溶液呈碱性,pH>7,选项A错误;
B、b点溶液中的溶质含有硫酸镁和硫酸2种,选项B错误;
C、由图像可知:氢氧化镁的质量为52.4g-46.6g=5.8g,MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓,则产生硫酸钡的质量为=![]() ,则m的质量为23.3g+5.8g=29.1g,选项C错误;
,则m的质量为23.3g+5.8g=29.1g,选项C错误;
D、加入硫酸后产生硫酸钡的质量=52.4g-29.1g=23.3g,则一共产生硫酸钡的质量为23.3g+23.3g=46.6g,则氢氧化钡的质量=![]() ,氢氧化钡溶液溶质质量分数=
,氢氧化钡溶液溶质质量分数=![]() 34.2%,选项D正确。故选D。
34.2%,选项D正确。故选D。

【题目】某同学设计以下实验探究氧化铜能否作为过氧化氢分解制取氧气的催化剂,以及影响化学反应速率的因素。
实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | 催化剂种类及用量/g | 氧气体积/mL | 收集氧气所用时间/s |
① | 5 | 10 | 20 | 无 | 100 | - |
② | 5 | 10 | 20 | 二氧化锰1g | 100 | 15 |
③ | 5 | 10 | 40 | 二氧化锰1g | 100 | 8 |
④ | 10 | 10 | 20 | 二氧化锰1g | 100 | 5 |
⑤ | 5 | 10 | 20 | 氧化铜1g | 100 | 22 |
(1)通过实验____和____对比,说明过氧化氢分解的速率与温度有关。
(2)通过实验____和____对比,说明过氧化氢分解的速率与浓度有关。
(3)通过实验____和____对比,说明氧化铜粉末能加快过氧化氢分解速率。
(4)想要证明氧化铜是该反应的催化剂,还需要验证其在反应前后____和____没有发生改变。
(5)①写出氧化铜催化过氧化氢分解的文字表达式:__________。
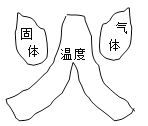
②根据以上实验得出的结论,在下图中画出有、无氧化铜时过氧化氢分解产生氧气的质量与反应时间的关系图____________。