题目内容
(2012?绵阳)(1)某简单粒子的结构示意图可表示为:
当x=8时,该粒子符号为 ;当x=10时,该粒子符号为 ;当x=13时,写出该粒子的硫酸盐的化学式为: ;
(2)t℃时,将5.2gKNO3固体溶于20.0g水中,刚好形成饱和溶液.t℃时,KNO3的溶解度为 .
(3)久置在空气中的氢氧化钠溶液,会生成一种盐类杂质,向其中加入稀盐酸时会产生无色气体.生成这种杂质的化学方程式为: ;向氢氧化钠溶液中滴入几滴酚酞试剂,溶液会变 .
(4)“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料,受热可分解为三种常见的化合物,物质转化关系如图,其中A是最常见的液态物质,B是黑色固体,F、G为金属单质.根据推断回答下列问题:

①H的化学式是 ;
②碱式碳酸铜[Cu2(OH)2CO3]中铜元素与氧元素的质量之比为: ;
③写出D+F→G+H反应的化学方程式: ;
④向Cu2(OH)2CO3]中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式: .

当x=8时,该粒子符号为 ;当x=10时,该粒子符号为 ;当x=13时,写出该粒子的硫酸盐的化学式为: ;
(2)t℃时,将5.2gKNO3固体溶于20.0g水中,刚好形成饱和溶液.t℃时,KNO3的溶解度为 .
(3)久置在空气中的氢氧化钠溶液,会生成一种盐类杂质,向其中加入稀盐酸时会产生无色气体.生成这种杂质的化学方程式为: ;向氢氧化钠溶液中滴入几滴酚酞试剂,溶液会变 .
(4)“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料,受热可分解为三种常见的化合物,物质转化关系如图,其中A是最常见的液态物质,B是黑色固体,F、G为金属单质.根据推断回答下列问题:

①H的化学式是 ;
②碱式碳酸铜[Cu2(OH)2CO3]中铜元素与氧元素的质量之比为: ;
③写出D+F→G+H反应的化学方程式: ;
④向Cu2(OH)2CO3]中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式: .
(1)O2﹣; Ne; Al2(SO4)3;
(2)26.0g.(3)Na2CO3+2HCl=2NaCl+CO2↑+H2O; 红色.
(4)①FeSO4;②8:5;
③Fe+CuSO4=FeSO4+Cu;
④4HCl+Cu2(OH)2CO3=2CuCl2+CO2↑+3H2O.
(2)26.0g.(3)Na2CO3+2HCl=2NaCl+CO2↑+H2O; 红色.
(4)①FeSO4;②8:5;
③Fe+CuSO4=FeSO4+Cu;
④4HCl+Cu2(OH)2CO3=2CuCl2+CO2↑+3H2O.
(1)某简单粒子的结构示意图可表示为: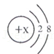
当x=8时,该粒子符号为 O2﹣;当x=10时,该粒子符号为Ne;当x=13时,该微粒为铝,在化合物中显+3价,而硫酸根显﹣2价,根据化合价的代数和为零,可得其化学式为:Al2(SO4)3;
(2)t℃时,将5.2gKNO3固体溶于20.0g水中,刚好形成饱和溶液.则100g水对应的硝酸钾质量为5.2g×5=26.0g,即t℃时,KNO3的溶解度为26.0g.
(3)久置在空气中的氢氧化钠溶液,会生成一种盐类杂质,向其中加入稀盐酸时会产生无色气体.反应生成氯化钠和水以及二氧化碳,方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;向氢氧化钠溶液中滴入几滴酚酞试剂,由于氢氧化钠溶液显碱性,所以溶液会变 红色.
(4)“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料,受热可分解为三种常见的化合物,物质转化关系如图,其中A是最常见的液态物质,为水,B是黑色固体是黑色的氧化铜.则B和硫酸反应生成的D为硫酸铜,而A确定为水(B和硫酸反应生成AD,这个方向很容易忽略).F、G为金属单质,且F和硫酸铜反应得到金属G,所以为F为活泼金属,而F来源于E和氧化铁的反应,所以F为铁.
①H的化学式是 FeSO4;
②碱式碳酸铜[Cu2(OH)2CO3]中铜元素与氧元素的质量之比为:8:5;
③写出D+F→G+H反应的化学方程式:Fe+CuSO4=FeSO4+Cu;
④向Cu2(OH)2CO3]中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式:4HCl+Cu2(OH)2CO3=2CuCl2+CO2↑+3H2O.

当x=8时,该粒子符号为 O2﹣;当x=10时,该粒子符号为Ne;当x=13时,该微粒为铝,在化合物中显+3价,而硫酸根显﹣2价,根据化合价的代数和为零,可得其化学式为:Al2(SO4)3;
(2)t℃时,将5.2gKNO3固体溶于20.0g水中,刚好形成饱和溶液.则100g水对应的硝酸钾质量为5.2g×5=26.0g,即t℃时,KNO3的溶解度为26.0g.
(3)久置在空气中的氢氧化钠溶液,会生成一种盐类杂质,向其中加入稀盐酸时会产生无色气体.反应生成氯化钠和水以及二氧化碳,方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;向氢氧化钠溶液中滴入几滴酚酞试剂,由于氢氧化钠溶液显碱性,所以溶液会变 红色.
(4)“孔雀石”的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它是一种重要的铜矿石原料,受热可分解为三种常见的化合物,物质转化关系如图,其中A是最常见的液态物质,为水,B是黑色固体是黑色的氧化铜.则B和硫酸反应生成的D为硫酸铜,而A确定为水(B和硫酸反应生成AD,这个方向很容易忽略).F、G为金属单质,且F和硫酸铜反应得到金属G,所以为F为活泼金属,而F来源于E和氧化铁的反应,所以F为铁.
①H的化学式是 FeSO4;
②碱式碳酸铜[Cu2(OH)2CO3]中铜元素与氧元素的质量之比为:8:5;
③写出D+F→G+H反应的化学方程式:Fe+CuSO4=FeSO4+Cu;
④向Cu2(OH)2CO3]中加入足量的盐酸,固体完全溶解,有无色气体生成,写出此反应的化学方程式:4HCl+Cu2(OH)2CO3=2CuCl2+CO2↑+3H2O.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
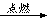 H2O
H2O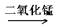 H2O + O2
H2O + O2 ” 。方程式中最后一种物质的化学式印刷不清楚,小明根据上下文了解到该物质是一种常见的酸,请根据已学知识推测其化学式: ,KMnO4中Mn元素化合价为 ,
” 。方程式中最后一种物质的化学式印刷不清楚,小明根据上下文了解到该物质是一种常见的酸,请根据已学知识推测其化学式: ,KMnO4中Mn元素化合价为 ,