题目内容
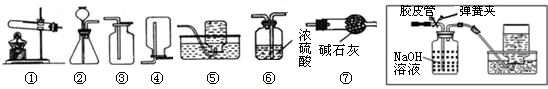
以下是我们熟悉的实验室制取气体的发生装置、收集装置以及净化装置(装置⑦中碱石灰为固体氢氧化钠和氧化钙的混合物).请根据装置图回答下列问题:

(1)将装置①中的固体加热时应先
(2)甲同学在实验室用大理石与稀盐酸反应制取CO2,应选用的装置组合是
(3)实验室用过氧化氢溶液和二氧化锰制氧气时,选用的发生装置为
(4)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气.通常情况下氨气密度比空气小且极易溶于水.欲制得干燥的氨气,装置的连接顺序为

(1)将装置①中的固体加热时应先
进行预热
进行预热
;装置①试管口向下倾斜的原因是防止水倒流而炸裂试管
防止水倒流而炸裂试管
;若用装置⑥净化气体,则气体应从b
b
端通入(填“a”或“b”).(2)甲同学在实验室用大理石与稀盐酸反应制取CO2,应选用的装置组合是
②③
②③
.(3)实验室用过氧化氢溶液和二氧化锰制氧气时,选用的发生装置为
②
②
、收集装置为③或⑤
③或⑤
(填装置编号),过氧化氢溶液从长颈漏斗
长颈漏斗
(填仪器名称)中加入.反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气.通常情况下氨气密度比空气小且极易溶于水.欲制得干燥的氨气,装置的连接顺序为
①⑦④
①⑦④
(填装置编号)分析:给试管中的固体加热的注意事项有:进行预热;试管口略向下倾斜,目的是防止水倒流而炸裂试管;若用装置⑥净化气体,则气体应从长管进入,即b端进入;制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,因此需要加热;氨气密度比空气小且极易溶于水,因此只能用向下排空气法收集;氨气不能用浓硫酸干燥,能用碱石灰干燥.
解答:解:(1)给试管中的固体加热的注意事项有:进行预热;试管口略向下倾斜,目的是防止水倒流而炸裂试管;若用装置⑥净化气体,则气体应从长管进入,即b端进入;故答案为:进行预热;防止水倒流而炸裂试管;b;
(2)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.故答案为:②③
(3)制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;液体药品从长颈漏斗中加入;故答案为:②;③或⑤;长颈漏斗;2H2O2
2H2O+O2↑;
(4)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,因此需要加热;氨气密度比空气小且极易溶于水,因此只能用向下排空气法收集;氨气不能用浓硫酸干燥,能用碱石灰干燥,故答案为:①⑦④
(2)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.故答案为:②③
(3)制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;液体药品从长颈漏斗中加入;故答案为:②;③或⑤;长颈漏斗;2H2O2
| ||
(4)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,因此需要加热;氨气密度比空气小且极易溶于水,因此只能用向下排空气法收集;氨气不能用浓硫酸干燥,能用碱石灰干燥,故答案为:①⑦④
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目