题目内容
【题目】已知固体混合物A是由氯化钾、硝酸钾、碳酸钡中的两种或几种组成;另有固体混合物B是由氯化铵、硝酸镁、氯化铜中的两种或几种组成。按下图所示进行实验出现的现象如图所示(设过程中所有发生的反应都恰好完全进行)。
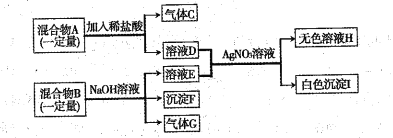
试根据实验过程判断,填空:
(1)若将气体C和气体G分别通入紫色石蕊试液后,试液变红,原气体是__________(写化学式);
(2)混合物B中一定含有___________(写化学式)
(3)沉淀F的组成可能有_________种(填写数字);
(4)无色溶液H中一定含有的金属阳离子是____________。
【答案】CO2 NH4Cl 3 K+、Na+、Ba2+
【解析】
碳酸钡和盐酸反应生成氯化钡、水和二氧化碳。氯化铵和氢氧化钠反应会生成氯化钠、水和氨气。镁离子和氢氧根离子反应生成氢氧化镁沉淀,氢氧根离子和铜离子会生成氢氧化铜沉淀。氯离子和银离子反应会生成氯化银沉淀。所以混合物A中加入稀盐酸会生成气体C,所以A中一定有碳酸钡,C是二氧化碳,混合物B中加入氢氧化钠会生成气体G和沉淀F,所以混合物B种含有氯化铵,可能含有硝酸镁和硝酸铜中一种或两种。溶液D、E中都含有氯离子。
(1)通过分析可知,若气体C和气体G分别通入紫色石蕊试液后,试液变红,原气体是CO2。故答案为:CO2;
(2)通过分析可知,混合物B中一定含有氯化铵。故答案为:NH4Cl;
(3)通过分析可知,沉淀F的组成可能只含有氢氧化铜,只含有氢氧化镁,可能含有氢氧化铜和氢氧化镁,共3种可能。故答案为:3;
(4)通过分析可知,无色溶液H中一定含有的金属阳离子是:K+、Ba2+、Na+。故答案为:K+、Ba2+、Na+。

【题目】我们知道,空气中氧气约占总体积的1/5,物质燃烧与空气中氧气密切相关。为此,小华进行了相关实验探究:
(实验探究)小华利用下列装置进行实验:
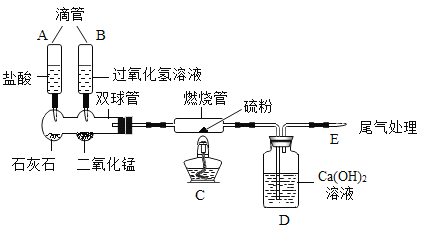
(实验操作及记录)(请你补充完整实验二)
实验 | 操作 | 现象 |
实验一 | 点燃酒精灯 | 硫燃烧,发出微弱的淡蓝色火焰 |
实验二 | 1.更换燃烧管(装有等量硫粉),挤压滴管A当观察到_____的现象时,可认为空气已经排尽 2.点燃酒精灯 | 硫没有燃烧 |
实验三 | 1.更换燃烧管(装有等量硫粉),挤压滴管B 2.当E处能使带火星的木条复燃时点燃酒精灯 | 硫燃烧很旺,发出明亮的蓝紫色火焰 |
(结果分析)
(1)对照实验一和实验_____的现象,说明硫燃烧需要氧气。
(2)对照实验三和实验一的现象,可知燃烧的剧烈程度与_____有关。
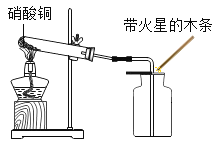
(交流与反思)小华为了进一步探究“是否只有纯氧才能使带火星的木条复燃”,又进行了以下实验:利用如图装置收集4瓶气体(集气瓶预先装满水,量筒规格为100mL),以带火星的木条进行检验。结果如下:

1号瓶 | 2号瓶 | 3号瓶 | 4号瓶 |
34mL O2+66mL 空气 | 35mL O2+65mL 空气 | 36mL O2+64mL 空气 | 37mL O2+63mL 空气 |
不复燃 | 不复燃,但很亮 | 很亮,复燃 | 立即复燃 |
据此可知,当O2的体积分数达到_____时(精确到1%),即可使带火星的小木条复燃。
(拓展资料)提供资料:
1.相同条件下,两种气体的体积比等于分子个数比。
2.硝酸铜固体加热分解生成氧化铜、二氧化氮和氧气。小华利用如图实验加热硝酸铜,发现收集的气体能使带火星木条复燃。请你根据该反应的化学方程式分析判断NO2_____(填“有”“无”或“无法确定”)助燃性。
【题目】在一个密闭容器内有四种物质,在一定条件下完全反应后,测得反应前后各物质的质量如下:
物质 | X | Y | Z | Q |
反应前质量/g | 4 | 10 | 1 | 21 |
反应后质量/g | 0 | 12 | 15 | 待测 |
已知X的相对分子质量为N,Q的相对分子质量为2N,下列推理正确的是( )
A. 反应后Q的质量为9 g
B. 反应中Y与Q发生改变的质量之比为1∶1
C. 反应后生成15 g Z
D. X与Q反应前的化学计量数之比为2∶1