题目内容
认真观察A、B两装置,写出B装置中发生反应的化学方程式 ,水中氢元素和氧元素的质量比为 -;用分子和原子的观点分析比较A装置和B装置在
试验过程中水的变化情况:A中 -;B中 。

【答案】
2H2O 2H2↑+O2↑
1:8 A中水分子本身没有改变,改变的是分子之间的间隔 B中水分子发生了改变,变成了氢气分子和氧气分子。
2H2↑+O2↑
1:8 A中水分子本身没有改变,改变的是分子之间的间隔 B中水分子发生了改变,变成了氢气分子和氧气分子。
【解析】
试题分析: B装置为电解水,水在通电条件下分解成氢气和氧气,反应的化学方程式为2H2O 2H2 ↑+O2↑ ;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
2H2 ↑+O2↑ ;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
考 点: 电解水实验;利用分子与原子的性质分析和解决问题;元素质量比的计算;书写化学方程式、文字表达式、电离方程式.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
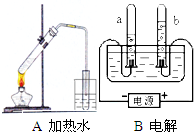 据图回答:
据图回答: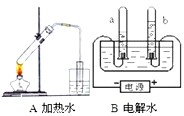 认真观察A、B两装置,回答下列问题:
认真观察A、B两装置,回答下列问题: 认真观察A、B两装置图,并填空.
认真观察A、B两装置图,并填空.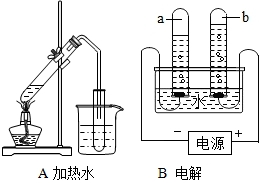 认真观察A、B两装置:
认真观察A、B两装置: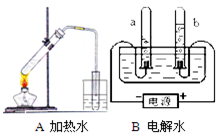 据图回答:
据图回答: