题目内容
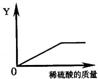
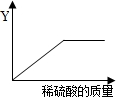
向一过量稀硫酸中加入一定量的锌粉,如图是反应过程中某种物质的质量Y随着锌粉的加入质量变化的关系,则Y不可能表示( )
A.消耗锌粉的质量
B.生成硫酸锌的质量
C.生成氢气的质量
D.溶液的总质量
【答案】分析:通过锌与稀硫酸反应的化学方程式分别估算锌粉、硫酸锌、氢气和溶液的总质量,再分别让锌粉的质量、硫酸锌的质量、氢气的质量和溶液的总质量在反应开始时、反应进行中和反应结束后对应在坐标系中,就能得出相应的图象,再与所给图象对照,即可得到答案.
解答:解:A、消耗掉的锌应该是从0慢慢增加的,这个不可以理解为是烧杯中剩余的锌,所以该图符合.
B、硫酸锌在反应开始时的质量为零,反应中硫酸锌的质量逐渐增加,由于稀硫酸过量,因此当锌粉全部反应后,硫酸锌的质量就增加到最大值,从而不再变化,所以对应的图象应该是一条从原点出发,先上升,再保持水平的一条曲线.所以该图符合.
C、氢气在反应开始时的质量为零,反应中氢气的质量逐渐增加,由于稀硫酸过量,因此当锌粉全部反应后,氢气的质量就增加到最大值,从而不再变化,所以对应的图象应该是一条从原点出发,先上升,再保持水平的一条曲线.所以该图符合.
D、由于是向硫酸中加入锌,所以开始时就是硫酸溶液的质量,所以不能为零,随着时间的进行,溶液质量在增加,当锌完全反应后质量不在增加.所以起点从0开始错误.
故选D
点评:本题主要考查有关化学方程式的计算和图象的表达.解答这类题目的关键首先是根据化学方程式计算或估算出相关的数据,然后再用图象表示出来,从而得到相关的答案.
解答:解:A、消耗掉的锌应该是从0慢慢增加的,这个不可以理解为是烧杯中剩余的锌,所以该图符合.
B、硫酸锌在反应开始时的质量为零,反应中硫酸锌的质量逐渐增加,由于稀硫酸过量,因此当锌粉全部反应后,硫酸锌的质量就增加到最大值,从而不再变化,所以对应的图象应该是一条从原点出发,先上升,再保持水平的一条曲线.所以该图符合.
C、氢气在反应开始时的质量为零,反应中氢气的质量逐渐增加,由于稀硫酸过量,因此当锌粉全部反应后,氢气的质量就增加到最大值,从而不再变化,所以对应的图象应该是一条从原点出发,先上升,再保持水平的一条曲线.所以该图符合.
D、由于是向硫酸中加入锌,所以开始时就是硫酸溶液的质量,所以不能为零,随着时间的进行,溶液质量在增加,当锌完全反应后质量不在增加.所以起点从0开始错误.
故选D
点评:本题主要考查有关化学方程式的计算和图象的表达.解答这类题目的关键首先是根据化学方程式计算或估算出相关的数据,然后再用图象表示出来,从而得到相关的答案.

练习册系列答案
相关题目