题目内容
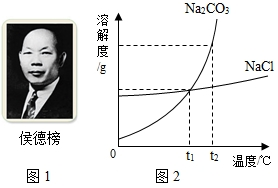
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl;②2NaHCO3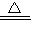 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;试回答下列问题:
(1)在反应①的六种物质中,焙制糕点是时常用作发酵粉的是 ;
(2)胺盐水比食盐水更容易吸收二氧化碳的原因是 .
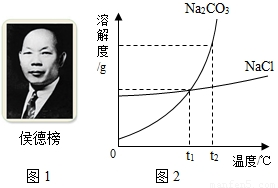
(3)氯化钠和碳酸钠的溶解度如图2,t2℃时,氯化钠饱和溶液溶质的质量分数 碳酸钠饱和溶液溶质的质量分数
(填“大于”“小于”“等于”之一).
(4)生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,说明这句谚语的原理: .
【答案】分析:(1)碳酸氢钠在焙制糕点时常用作发酵粉.
(2)氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳.
(3)根据饱和溶液溶质质量分数= ×100%进行分析.
×100%进行分析.
(4)根据碳酸钠和氯化钠的溶解度随温度的变化情况来判断结晶的方法.
解答:解:(1)碳酸氢钠在焙制糕点时常用作发酵粉,故答案为:碳酸氢钠;
(2)氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳,故答案为:氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳;
(3)t2℃时,氯化钠的溶解度小于碳酸钠的溶解度,根据饱和溶液溶质质量分数= ×100%可知,t2℃时,氯化钠的饱和溶液中溶质的质量分数小于碳酸钠的饱和溶液中溶质的质量分数,故答案为:小于;
×100%可知,t2℃时,氯化钠的饱和溶液中溶质的质量分数小于碳酸钠的饱和溶液中溶质的质量分数,故答案为:小于;
(4)氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出,故答案为:氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出.
点评:本题难度不是很大,主要考查了碳酸氢钠的用途、饱和溶液中溶解度的计算以及根据固体的溶解度曲线解决相关的问题等,培养分析问题、解决问题的能力.
(2)氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳.
(3)根据饱和溶液溶质质量分数=
 ×100%进行分析.
×100%进行分析.(4)根据碳酸钠和氯化钠的溶解度随温度的变化情况来判断结晶的方法.
解答:解:(1)碳酸氢钠在焙制糕点时常用作发酵粉,故答案为:碳酸氢钠;
(2)氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳,故答案为:氨气溶于水呈碱性,更容易吸收酸性氧化物二氧化碳;
(3)t2℃时,氯化钠的溶解度小于碳酸钠的溶解度,根据饱和溶液溶质质量分数=
 ×100%可知,t2℃时,氯化钠的饱和溶液中溶质的质量分数小于碳酸钠的饱和溶液中溶质的质量分数,故答案为:小于;
×100%可知,t2℃时,氯化钠的饱和溶液中溶质的质量分数小于碳酸钠的饱和溶液中溶质的质量分数,故答案为:小于;(4)氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出,故答案为:氯化钠的溶解度随湿度变化不大,由于夏天气温高,水分蒸发快,氯化钠易结晶斩出;纯碱的溶解度随温度的变化大,冬天气温很低,使碳酸钠结晶析出.
点评:本题难度不是很大,主要考查了碳酸氢钠的用途、饱和溶液中溶解度的计算以及根据固体的溶解度曲线解决相关的问题等,培养分析问题、解决问题的能力.

练习册系列答案
相关题目
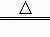 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;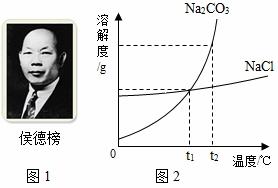
 碱”,请结合溶解度曲线,说明这句谚语的原理:
碱”,请结合溶解度曲线,说明这句谚语的原理:  .
. Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;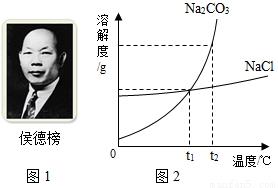
 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;