题目内容
【题目】某化学兴趣小组对酸、碱、盐的部分性质进行探究。
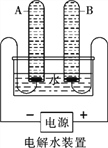
(探究一)证明氢氧化钠与二氧化碳能发生反应。
甲同学按如图装置进行实验:
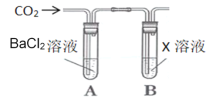
(1)已知CO2与BaCl2不反应,为证明NaOH与CO2能反应,X溶液中的溶质应该是____(填化学式);
(2)能证明NaOH与CO2能反应的实验现象是_________________________;
(探究二)氢氧化钠在空气中变质的程度?
(3)乙同学取少量久置的氢氧化钠样品于试管中,加水溶解,然后滴加几滴稀盐酸,发现没有气泡产生,根据此现象_____(填“能”或“不能”)判断氢氧化钠是否变质,其原因是__________。
(4)丙同学对该氢氧化钠变质的程度作出如下两个猜想,并按下图进行实验:
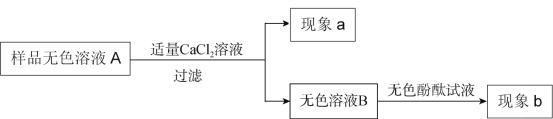
猜想1:全部变质(Na2CO3); 猜想2:部分变质(NaOH和Na2CO3);
①现象a为白色沉淀,产生此现象的化学方程式为____________________;
②若现象b为无色溶液B变红色,综合①②可知猜想_______成立;
(探究三)碳酸钠能否与二氧化碳反应?
(查阅资料)①溶洞中的石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成可溶于水的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2;
②碳酸氢钠溶液呈碱性;
碳酸钠溶液中通入一定量二氧化碳,是否能生成碳酸氢钠(NaHCO3)?于是丁同学开始实验探究 (不考虑二氧化碳和碳酸作为溶质的情况) 。
(提出问题)所得溶液中所含溶质成分是什么?
(提出猜想)猜想一:溶质为Na2CO3;猜想二:溶质为NaHCO3;猜想三:溶质为____________。
(设计实验)
实验操作 | 实验现象 | 实验结论 |
①取所得溶液少许于试管中,向其中滴加过量的CaCl2溶液 | 有白色沉淀生成 | 猜想二________ (选填“成立”或“不成立”) |
②取实验步骤①中上层清液,滴加适量稀盐酸 | _______________ | 猜想一不成立 |
(得出结论)猜想三成立,证明二氧化碳通入碳酸钠溶液生成了碳酸氢钠。写出实验步骤②中发生反应的化学方程式:____________________________。
(讨论交流)小明同学认为,向碳酸钠溶液中通入一定量二氧化碳后,再向所得溶液中滴加几滴酚酞溶液。溶液变红就能证明一定有碳酸氢钠生成;小红同学对小明同学的结论产生怀疑,其理由是___________________________。
【答案】BaCl2、NaOH B中产生白色沉淀 不能 若有少量氢氧化钠变质,当加入少量盐酸后,只与氢氧化钠反应,不会产生气泡 Na2CO3+CaCl2=CaCO3![]() +2NaCl 2 Na2CO3、NaHCO3 不成立 有气泡冒出 NaHCO3+HCl=NaCl+H2O+CO2↑ 碳酸钠溶液显碱性,也能使酚酞试液变红色
+2NaCl 2 Na2CO3、NaHCO3 不成立 有气泡冒出 NaHCO3+HCl=NaCl+H2O+CO2↑ 碳酸钠溶液显碱性,也能使酚酞试液变红色
【解析】
[探究一](1)CO2与BaCl2不反应,NaOH与CO2反应生成的碳酸钠可以和BaCl2反应生成碳酸钡沉淀,而BaCl2和 NaOH不反应,X溶液中的溶质应该是BaCl2、 NaOH;
(2)NaOH与CO2反应生成的碳酸钠可以和BaCl2反应生成碳酸钡白色沉淀,可以证明NaOH能与CO2反应;
[探究二] (3)氢氧化钠变质,是因为氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;若有少量氢氧化钠变质,当加入少量盐酸后,只与氢氧化钠反应,不会产生气泡,所以不能判断氢氧化钠是否变质;
(4)①Na2CO3能和CaCl2反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:Na2CO3+CaCl2=CaCO3![]() +2NaCl;
+2NaCl;
②向无色溶液A中加入适量CaCl2溶液后,Na2CO3能和CaCl2完全反应生成碳酸钙沉淀和氯化钠,现象a为白色沉淀,说明有Na2CO3;向无色溶液B中加入酚酞溶液,溶液变红,说明有NaOH,因而证明猜想2成立;
[探究三] [提出猜想] 猜想一,溶质为Na2CO3;猜想二:溶质为NaHCO3;由以上猜想可知,猜想三:溶质为Na2CO3、NaHCO3;
[设计实验] ①取所得溶液少许于试管中,向其中滴加过量的CaCl2溶液,产生白色沉淀,说明溶液中含有碳酸钠;
②取实验步骤①中上层清液,滴加适量稀盐酸,产生气泡,说明溶液中含有碳酸氢钠;
[得出结论] 实验步骤②中,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
[讨论交流] 小红同学对小明同学的结论产生质疑,其理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。

【题目】科学方法对化学学习起着事半功倍的作用。
(1)分类归纳是研究化学物质的重要方法。如图是某同学整理的碳及其化合物的知识网络图,转化③常用于冶炼工业,工业上用赤铁矿炼铁时,反应的化学方程式为_____,二氧化碳使紫色石蕊试液变红涉及的反应是如图所示转化中_____(填序号)。
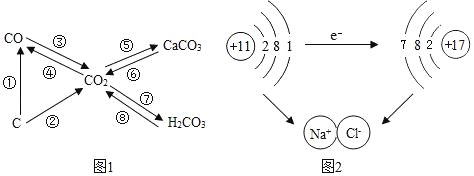
(2)微观粒子模型化是研究化学变化的重要方法。
①如图是钠与氯气反应生成氯化钠的示意图。该图说明在化学反应过程中一定发生变化的是_____(填字母)。
A 原子核 B 原子核最外层电子数 C 原子的电子层数
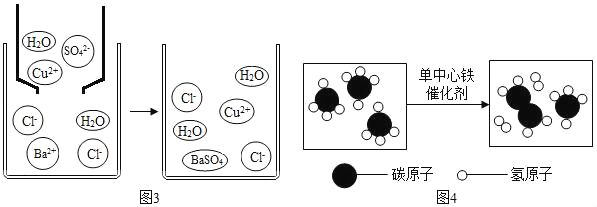
②如图是硫酸铜溶液与氯化钡溶液反应示意图。从粒子角度分析该化学反应能发生的原因是_____。
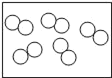
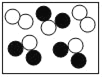
③A、B、C、D表示4种物质,如图是部分物质的微观示意图。A和B在一定条件下反应生成C和D.
物质 | B | C | D |
|
微观示意图 |
|
|
|
一定质量的A和4.8g B恰好完全反应,可生成4.4gC和2.7gD,则A的化学式是_____。
④我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。甲烷转化反应的微观示意图如图:
图示所表示的反应的化学方程式为_____。
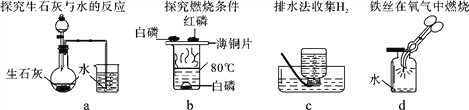
(3)控制变量、设计对比实验是实验探究的重要方法。

如图实验是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论不正确的是_____(填字母)。
A 铜不能发生置换反应
B 四种金属中金属活动性最强的是Mg
C 等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多
【题目】将足量物质乙加入物质甲中,加入物质乙的质量与纵坐标y的关系不能用如图所示曲线表示的是( )
选项 | 甲 | 乙 | 纵坐标y |
A | 硝酸铜与硝酸银的混合溶液 | 锌粉 | 红色固体质量 |
B | 氯化铁与稀盐酸的混合溶液 | 氢氧化钠 | 沉淀质量 |
C | 不饱和氯化钠溶液 | 硝酸钾 | 溶质质量分数 |
D | 久置于空气中的氢氧化钠溶液 | 稀盐酸 | 气体质量 |
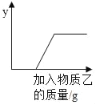
A. AB. BC. CD. D
【题目】已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | |
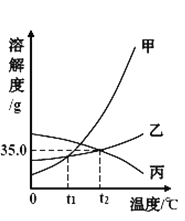
依据上表数据和溶解度曲线判断,下列说法错误的是
A. 能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B. t1℃时,氯化钾和硝酸钾的溶解度相等,在 34.0 g 至 35.0 g 之间
C. t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D. 氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯