题目内容
【题目】硅钢可用于制造变压器的铁芯。某化学兴趣小组的同学为了分析硅钢(主要含有Fe、C、Si)的成分,设计了如下的实验流程(有些反应的部分反应物和生成物已省略)。查阅资料发现:常温下单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应。(Si+2NaOH+H2O=Na2SiO3+2H2↑)
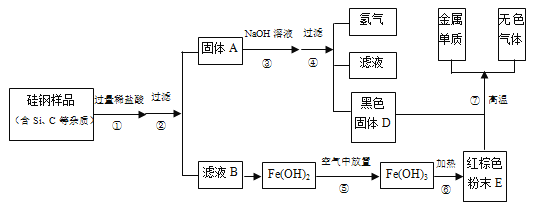
根据以上信息,回答下列问题:
(1)固体A的成分为 ,滤液B中的金属阳离子为 ;
(2)写出步骤⑦中发生反应的化学方程式 ;
(3)步骤⑤中发生的是化合反应,尝试写出其化学方程式 。
【答案】(1)Si和C Fe2+(2)3C + 2Fe2O3 ![]() 4Fe + 3CO2↑
4Fe + 3CO2↑
(3)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
【解析】
试题分析:(1)硅钢(主要含有Fe、C、Si),加入盐酸,Fe + 2HCl == FeCl2 + H2↑,而C、Si不会仍是固体且不溶于水,因此固体A含C、Si ;滤液B中溶质为未反应的HCl和生成的FeCl2 ,因此金属阳离子为Fe2+;(2)步骤⑦中为黑色固体C和红棕色粉末Fe2O3 在高温条件下发生的还原反应;

 互动英语系列答案
互动英语系列答案【题目】结合下列实验装置图回答问题:
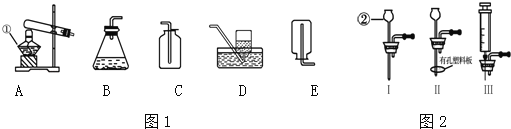
(1)装置B虽然操作简便,但无法控制反应速率.请从图2中选取 (填序号)取代B中的单孔塞,以达到控制反应速率的目的.同样能控制反应进行和停止的是 .
(2)“化学反应条件的控制是实验的灵魂”.某校化学兴趣小组在老师指导下,进行了“影响双氧水(过氧化氢溶液)分解因素”的探究实验.下表是该化学兴趣小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2溶液制取150mL氧气所需的时间(秒)
反应条件\浓度 | 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
1无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
2无催化剂、加热 | 360 | 480 | 540 | 720 |
3MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
①该研究小组在设计方案时.考虑了浓度、催化剂、 等因素对过氧化氢分解速率的影响.
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响 .
③用化学变化文字表达式表示上述表格3中的反应 .


