题目内容
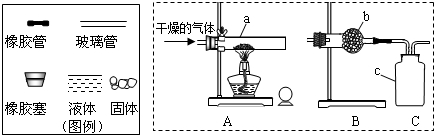
下图是实验室制取CO2,并验证CO2和CO的性质的实验,请看图后回答问题.
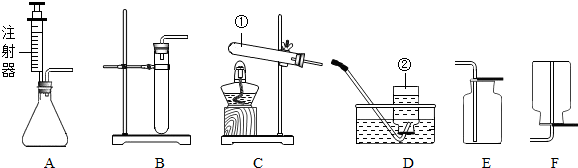
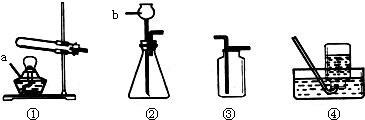
(1)写出标有序号的仪器名称①
(2)A中所观察到的现象是
反应方程式为
(3)B中所观察到的现象是
反应方程式为
(4)C中所观察到的现象是
反应方程式为
(5)D中所观察到的现象是
反应的化学方程式为
(6)E中所观察到的现象是
反应方程式为
分析:题中图是实验室制取CO2,并验证CO2和CO的性质的实验:
(1)熟记常用仪器;(2)用碳酸钙和盐酸制取二氧化碳;(3)二氧化碳和碳高温下反应生成一氧化碳;(4)一氧化碳还原黑色固体氧化铜,生成红色的铜;(5)检验生成的气体是否为二氧化碳;(6)点燃尾气,防止污染空气.
(1)熟记常用仪器;(2)用碳酸钙和盐酸制取二氧化碳;(3)二氧化碳和碳高温下反应生成一氧化碳;(4)一氧化碳还原黑色固体氧化铜,生成红色的铜;(5)检验生成的气体是否为二氧化碳;(6)点燃尾气,防止污染空气.
解答:解:(1)熟记常用仪器:长颈漏斗、铁架台;
(2)制取二氧化碳:①现象为:有大量气泡产生,固体逐渐减少;②化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O (3)一氧化碳与碳反应:①现象黑色固体逐渐减少;②化学方程式CO2+C
2CO;
(4)还原氧化铜:①现象:黑色固体逐渐变为红色,固体逐渐减少;②化学方程式CO+CuO
Cu+CO2
(5)检验二氧化碳:①现象:澄清石灰水变浑浊;②化学方程式Ca(OH)2+CO2═CaCO3↓+H2O
(6)点燃尾气:①现象:气体燃烧,产生淡蓝色的火焰;②化学方程式2CO+O2
2CO2
故答为:(1)长颈漏斗、铁架台;
(2)有大量气泡产生,固体逐渐减少;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)黑色固体逐渐减少;CO2+C
2CO;
(4)黑色固体逐渐变为红色,固体逐渐减少;CO+CuO
Cu+CO2;
(5)澄清石灰水变浑浊;
Ca(OH)2+CO2═CaCO3↓+H2O;
(6)气体燃烧,产生淡蓝色的火焰;2CO+O2
2CO2
(2)制取二氧化碳:①现象为:有大量气泡产生,固体逐渐减少;②化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O (3)一氧化碳与碳反应:①现象黑色固体逐渐减少;②化学方程式CO2+C
| ||
(4)还原氧化铜:①现象:黑色固体逐渐变为红色,固体逐渐减少;②化学方程式CO+CuO
| ||
(5)检验二氧化碳:①现象:澄清石灰水变浑浊;②化学方程式Ca(OH)2+CO2═CaCO3↓+H2O
(6)点燃尾气:①现象:气体燃烧,产生淡蓝色的火焰;②化学方程式2CO+O2
| ||
故答为:(1)长颈漏斗、铁架台;
(2)有大量气泡产生,固体逐渐减少;CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)黑色固体逐渐减少;CO2+C
| ||
(4)黑色固体逐渐变为红色,固体逐渐减少;CO+CuO
| ||
(5)澄清石灰水变浑浊;
Ca(OH)2+CO2═CaCO3↓+H2O;
(6)气体燃烧,产生淡蓝色的火焰;2CO+O2
| ||
点评:本题主要考查二氧化碳的化学性质及应用,掌握二氧化碳的制取装置和原理,熟记一氧化碳的化学性质和一些常用的化学方程式;学会分析反应现象和本质的联系.

练习册系列答案
相关题目