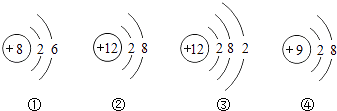题目内容
【题目】如图中A,B,C,D是四种粒子的结构示意图,E是银元素在元素周期表中的信息. 
请回答下列问题:
(1)图中A,B,C,D粒子共表示种元素.
(2)D中x= .
(3)E中银元素原子的质子数为 , 一个银原子质量是一个碳﹣12原子质量的倍.
(4)写出A中的粒子符号: .
【答案】
(1)三
(2)8
(3)47;9
(4)Al3+
【解析】解:(1)依据质子数不同元素种类不同,由图示可知四种微粒中共有质子数是13、17和18的三种元素;(2)由于原子中质子数与核外电子数相等,观察可知该微粒的质子数是18,是具有稳定结构的氩原子,所以核外电子数也应为18,所以X为8;(3)根据元素周期表中的一格中获取的信息,该元素的原子序数为47;根据原子序数=核电荷数=质子数,则银元素原子的质子数为47.相对原子质量与原子的实际质量成正,银的相对原子质量为108,他的相对原子质量为12,则一个银原子质量是一个碳12原子质量的108÷12=9倍.(4)阳离子是质子数大于核外电子数,故A是带有三个正电荷的铝离子:Al3+;
所以答案是:(1)三;(2)8;(3)47;9;(4)Al3+;

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
【题目】某反应中的甲、乙、丙、丁、戊在反应进行到不同程度时的物质的质量如下表:
甲/g | 乙/g | 丙/g | 丁/g | 戊/g | |
反应前 | 32 | 5 | a | ||
t时刻 | 16 | 16 | 5 | 9.5 | 4 |
反应后 | 0 | 27 | b | c | 0 |
则下列说法正确的是( )
A.若丙的化学性质在反应前后也不改变,则丙是该反应的催化剂
B.反应前a物质的质量一定为1.5g
C.该反应可能是CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
D.若丁与戊的化学计量数之比为2:1,则丁与戊的相对分子质量之比为9:4