题目内容
【题目】化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验。实验装置如下图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物)。
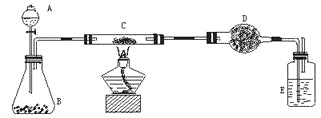
实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g。样品中铜的质量分数=[w-(b-a)×12/44]/w
请回答下列问题。
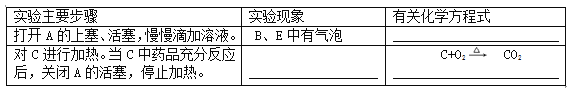
①主要实验内容
②实验讨论
装置E中盛放的试剂是 ,其作用是 。
按上述实验,得到铜的质量分数不精确,你认为是 (填:偏大、偏小、或不能确定),原因是 ,如果要得到了较正确的结果,对该装置改进的方法是 。
【答案】(12)2H2O2![]() 2H2O+O2↑(13)C中的灰红色粉末变成黑色 (14)2Cu+O2===2CuO
2H2O+O2↑(13)C中的灰红色粉末变成黑色 (14)2Cu+O2===2CuO
(15)澄清石灰水 (16)检验D装置是否完全吸收了二氧化碳 (17)偏小
(18) 水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大
(19)在装置B与C之间接一个与D相同的装置
【解析】试题分析: 滴加过氧化氢溶液,发生反应2H2O2![]() 2H2O+O2↑所以B、E中有气泡冒出,C中过量的C和生成的Cu与O2反应,即方程式为2Cu+O2===2CuO ,产生的现象为 C中的灰红色粉末变成黑色;D中盛放的是固体氢氧化钠和氧化钙的混合物,是作为干燥剂,可以吸收水蒸气和CO2;装置E中盛放的试剂是澄清石灰水,检验D装置是否完全吸收了二氧化碳;按上述实验,就会把水蒸气算成二氧化碳的质量,得到C的质量增大,Cu的质量减小导致铜的质量分数偏小;故必须要把水蒸气先干燥掉,可以在装置B与C之间接一个与D相同的装置。
2H2O+O2↑所以B、E中有气泡冒出,C中过量的C和生成的Cu与O2反应,即方程式为2Cu+O2===2CuO ,产生的现象为 C中的灰红色粉末变成黑色;D中盛放的是固体氢氧化钠和氧化钙的混合物,是作为干燥剂,可以吸收水蒸气和CO2;装置E中盛放的试剂是澄清石灰水,检验D装置是否完全吸收了二氧化碳;按上述实验,就会把水蒸气算成二氧化碳的质量,得到C的质量增大,Cu的质量减小导致铜的质量分数偏小;故必须要把水蒸气先干燥掉,可以在装置B与C之间接一个与D相同的装置。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】同学们学习化学后可知,二氧化碳能使澄清的石灰水变浑浊(生成白色沉淀)。但同 学们在分组实验中,向石灰水中通入二氧化碳时(如图1所示),却出现了意想不到的现象: 有的石灰水未变浑浊;有的石灰水出现浑浊后又变澄清了(沉淀消失)。
【提出问题】分组实验中,出现意想不到现象的原因是什么呢?
【猜想与假设】
I.石灰水未变浑浊,是因为二氧化碳中混有少量氯化氢气体.
Ⅱ.石灰水未变浑浊,是因为____________________________________。
Ⅲ.石灰水出现浑浊后又变澄清,与石灰水的浓度、通入二氧化碳的时间有关。
【进行实验】实验装置如图2所示。
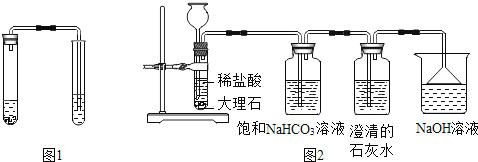
提示:①实验中所用盐酸与分组实验所用盐酸相同;
②CO2在饱和NaHCO3溶液中的溶解度非常小.
步骤1:分别取一定体积的饱和澄清石灰水与一定体积的蒸馏水混合配制成50mL溶液.
步骤2:分别向50mL溶液中通入一段时间的二氧化碳,记录现象.
实验序号 | V饱和石灰水/mL | V蒸馏水 /mL | 出现现象所需时间/s | |||
开始浑浊 | 明显浑浊 | 沉淀减少 | 是否澄清 | |||
① | 50 | 0 | 19 | 56 | 366 | 持续通入CO28min以上,沉淀不能完全消失 |
② | 40 | 10 | 24 | 51 | 245 | |
③ | 30 | 20 | 25 | 44 | 128 | |
④ | 20 | 30 | 27 | 35 | 67 | 89s后完全澄清 |
⑤ | 10 | 40 | 通3min以上,均无明显现象 | |||
【解释与结论】
(1)实验中,所用石灰水为饱和溶液的是______________(填序号).
(2)二氧化碳使澄清石灰水变浑浊原因是________________________________(用化学方程式表示).
(3)饱和NaHCO3液的作用是________________________.
(4)通过实验分析,猜想 I_______________(填“成立”或“不成立”),猜想Ⅱ、Ⅲ成立。
【反思与评价】
(5)向澄清的石灰水中通入二氧化碳,为避免出现“意想不到的现象”,你的建议是
__________________________________________________________________。