题目内容
用纯净的木炭粉末还原氧化铜粉末时,可发生的反应有:C + 2CuO=2Cu + CO2↑,C + CuO=Cu + CO↑。现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是
- A.CO2
- B.CO
- C.CO、CO2
- D.Cu、CO
C
试题分析:根据方程式的计算,可以判断全部生成二氧化碳需要氧化铜的质量和全部生成一氧化碳需要氧化铜的质量,并对二者进行比较即可。设参加反应的氧化铜的质量为X
C+2CuO 2Cu+CO2↑
2Cu+CO2↑
12 160
1.2g x
 解得x=16g
解得x=16g
C+CuO Cu+CO↑
Cu+CO↑
12 80
1.2g x
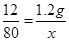 解得x=8g
解得x=8g
从方程式中的关系可以看出,1.2g的碳全部转化成二氧化碳需要氧化铜质量为16g,1.2g的碳全部转化成一氧化碳需要氧化铜为8g,而现在氧化铜的质量为10g,介于8g和16g之间,所以生成的气体既有二氧化碳,也有一氧化碳,故选C。
考点:本题考查根据化学反应方程式的计算
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力。
试题分析:根据方程式的计算,可以判断全部生成二氧化碳需要氧化铜的质量和全部生成一氧化碳需要氧化铜的质量,并对二者进行比较即可。设参加反应的氧化铜的质量为X
C+2CuO
 2Cu+CO2↑
2Cu+CO2↑12 160
1.2g x
 解得x=16g
解得x=16gC+CuO
 Cu+CO↑
Cu+CO↑12 80
1.2g x
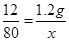 解得x=8g
解得x=8g从方程式中的关系可以看出,1.2g的碳全部转化成二氧化碳需要氧化铜质量为16g,1.2g的碳全部转化成一氧化碳需要氧化铜为8g,而现在氧化铜的质量为10g,介于8g和16g之间,所以生成的气体既有二氧化碳,也有一氧化碳,故选C。
考点:本题考查根据化学反应方程式的计算
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 =2Cu+CO2↑,C+CuO
=2Cu+CO2↑,C+CuO Cu+CO↑.现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是( )
Cu+CO↑.现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是( ) =2Cu+CO2↑,C+CuO
=2Cu+CO2↑,C+CuO Cu+CO↑.现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是( )
Cu+CO↑.现用1.2g木炭粉末还原10g氧化铜粉末,反应物刚好反应完全,则生成的气体产物是( )