题目内容
现有如下图所示的实验装置,请据图回答问题:
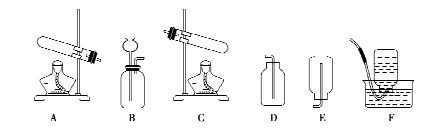
(1)如果用锌粒和稀硫酸反应来制取氢气,应选用的发生装置是______(填序号,下同),反应的方程式是_________________________________________。要想收集一瓶较纯净的氢气,最好选用装置_______来收集。
(2)实验室制取甲烷是用加热无水醋酸钠和碱石灰的固体混合物的方法,则制取甲烷应选择的发生装置是___________。
(3)实验室制取氧气时,使用B装置比A装置的优点是_______________________________。
【答案】
(1)B;H2SO4+Zn=ZnSO4+H2↑;F;(2)A;(3)操作简便,不用加热.
【解析】(1)金属锌是活泼金属,可与酸反应生成盐和氢气,锌粒和稀硫酸反应是硫酸锌和氢气,反应的方程式为:H2SO4+Zn=ZnSO4+H2↑;发生装置的特点属于固液常温的反应,故选择B装置;氢气的密度比空气小且难溶于水,所以收集氢气可以采用向下排空气法或排水法,但排水法收集的氢气较纯净;
(2)用无水醋酸钠和碱石灰两种固体混合物加热制取甲烷,故发生装置的特点属于固体加热型选择A装置作为发生装置;
(3)实验室制氧气时,B装置在常温下反应,而A装置需要加热,故使用B装置比A装置的优点是操作简便,不用加热;

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
现有如下图所示的实验装置:

现有稀硫酸、CuO、Fe粉三种物质,请设计两种制取铜的实验方案。填写下表。
| 实验方案 | 有关反应的化学方程式 | 选用装置(填 字母代号) |
| 方案一 | ||
| 方案二 |
在以上两个设计方案中,你认为__________操作更合理,更简便。