题目内容
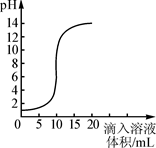
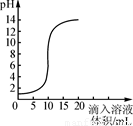
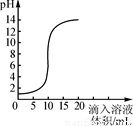
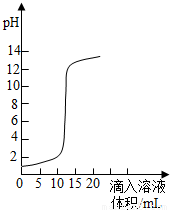
右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”或“小于”或“等于”)
(2)根据曲线图判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 .
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色.
【答案】分析:(1)强酸强碱恰好中和时,溶液显中性;
(2)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;
(3)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
解答:解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中,故答案为:氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH为1,酸性溶液;
(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红.
点评:酸碱中和反应结合图象知识来考查,难度较大,考查的知识面较广.
(2)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;
(3)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
解答:解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中,故答案为:氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH为1,酸性溶液;
(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红.
点评:酸碱中和反应结合图象知识来考查,难度较大,考查的知识面较广.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目