题目内容
一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末。
 【资料获悉】铁系“脱氧剂”的作用原理是利用铁能被氧气氧化,从而达到除氧保鲜的目的。
【资料获悉】铁系“脱氧剂”的作用原理是利用铁能被氧气氧化,从而达到除氧保鲜的目的。
【教师指导】铁被氧气氧化最终产物为红棕色的Fe2O3(其他产物忽略不计)。
【探究目的】小组同学欲探究该“脱氧剂”是否已经失效(即单质铁是否已经完全被氧化),并测定各成分的质量分数,设计了以下探究实验。
【实验探究】
步骤1:小刚用磁铁接近样品,发现磁铁吸引了部分黑色固体。
步骤2:称取10.00g样品于一烧杯中,加足量水充分搅拌溶解后,过滤,将滤渣洗涤、干燥、称得其质量为7.28g。
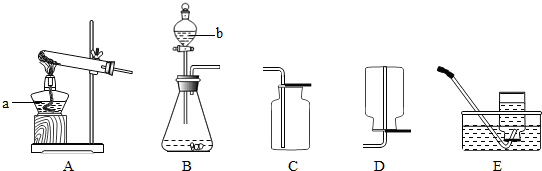
步骤3:如图,将得到的7.28g固体与足量稀硫酸反应,用电子秤称得反应前后总质量差为0.15g。
步骤4:将锥形瓶中反应后的液体过滤,并将滤渣洗涤、干燥后,称得其质量为1.20g。
【交流讨论】
(1)由步骤1得出的结论是_____________________________。
(2)步骤2的目的为了推测出“脱氧剂”含有_____(填物质的化学式),其质量为______。
(3)步骤3中仪器A的名称为 _____________。
小明认为0.15g差值即为H2的质量,并由此计算出样品中单质铁的质量为4.20g。
小华提出在装置的a导管处应该再连接一个盛有碱石灰(氧化钙和氢氧化钠固体的混合物)的干燥管,他这样做的目的是____________________。
(4)步骤4中滤渣是________(填化学式),如果没有经过洗涤,则称得的质量 _________1.20g(填“>”、“<”或“=”)。
【教师指导】样品在稀硫酸中除了Fe、Fe2O3分别能与稀硫酸反应外,还存在反应:
Fe+ Fe2(SO4)3=3FeSO4。因此,小明用产生H2的质量计算样品中铁的质量不合理。实际上,样品中单质铁的质量应该是与酸反应消耗的铁和与Fe2(SO4)3反应消耗铁的质量总和。
【学生实验】小红将步骤3的装置进行了改进,重新称取10.00g样品进行实验,并准确测得固体与足量稀硫酸反应前后总质量差为0.14g。
【数据处理】由于反应过程较复杂,小组同学在老师的帮助下,推算出与Fe2(SO4)3反应消耗铁的质量为0.56g。
【请你参与】(1)写出Fe2O3与稀硫酸反应的化学方程式。
(2)请根据以上数据,计算样品中Fe2O3的质量分数。
【交流讨论】
(1)样品中有单质铁存在
(2)NaCl 2.72g
(3)锥形瓶 吸收水蒸气,减少对H2质量测定产生误差
(4)C >
【请你参与】
(1)略
(2)16%