题目内容
(2012?铁岭)黄铜是铜和锌合金.某化学兴趣小组的同学在测定黄铜样品中铜的含量时,取黄铜样品20g放入烧杯中,向其中加入100g稀硫酸,恰好完全反应.反应后烧杯中剩余物的总质量为119.8g.请计算:
(1)反应产生氢气的质量是
(2)求黄铜样品中铜的质量分数.(写出计算过程)
(1)反应产生氢气的质量是
0.2
0.2
g.(2)求黄铜样品中铜的质量分数.(写出计算过程)
分析:根据黄铜的成分铜和锌的性质可知,加入稀硫酸时,只有锌与硫酸反应生成了硫酸锌和氢气;根据质量守恒定律,烧杯内质量的减少的质量即生成的氢气质量,据此根据反应的化学方程式列式计算出参加反应锌的质量,进而计算出铜的质量和铜的质量分数.
解答:解:(1)根据质量守恒定律,产生氢气的质量为:20g+100g-119.8g=0.2g.故答案为:0.2.
(2)设黄铜样品中锌的质量为x,
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
=
x=6.5g
黄铜样品中铜的质量分数为:
×100%=67.5%.
答:黄铜样品中铜的质量分数为67.5%.
(2)设黄铜样品中锌的质量为x,
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| x |
| 2 |
| 0.2g |
黄铜样品中铜的质量分数为:
| 20g-6.5g |
| 20g |
答:黄铜样品中铜的质量分数为67.5%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氢气的质量是正确解答本题的前提和关键.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
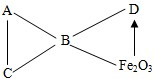 (2012?铁岭)现有铁、氧化铁、稀盐酸、氢氧化钙、碳酸钠五种物质,有如图所示的转化关系.图中“--”表示两端的物质可以发生化学反应,“→”表示可以由一种物质直接转化成另一种物质(部分反应物和生成物以及反应条件已经略去).请回答下列问题:
(2012?铁岭)现有铁、氧化铁、稀盐酸、氢氧化钙、碳酸钠五种物质,有如图所示的转化关系.图中“--”表示两端的物质可以发生化学反应,“→”表示可以由一种物质直接转化成另一种物质(部分反应物和生成物以及反应条件已经略去).请回答下列问题: