题目内容
【题目】元素化合物知识是初中化学重要的学习内容,请解答下列问题.
(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式: . 
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是 (填字母).
A.产生的气体可能是H2
B.产生的气体可能是CO2
C.CuSO4溶液中可能含有少量的某种酸
D.CuSO4溶液的pH 小于7
(3)某氯化钠溶液中含有较多CaCl2 , 按下图方案提纯得到氯化钠晶体. 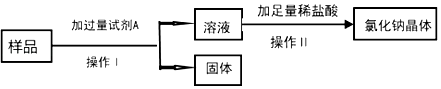
①试剂A的化学式为 .
②加入足量稀盐酸的目的是 .
③操作Ⅰ、Ⅱ的名称分别是、 .
④操作Ⅰ、Ⅱ中都要用到一种玻璃仪器,该仪器在操作Ⅱ中的作用是 .
(4)工业上常用电解饱和食盐水的方法制备氢氧化钠,产物除氢氧化钠外,还有氯气和氢气.若要制取200t氢氧化钠,理论上需要氯化钠的质量是多少?
【答案】
(1)4Al+3O2=2Al2O3
(2)B
(3)Na2CO3;除去过量的碳酸钠;过滤;蒸发;用玻璃棒不断搅拌,防止因局部温度过高,造成液滴飞溅
(4)解:设需要氯化钠的质量为x
2NaCl+2 H2O | 2NaOH+H2↑+Cl2↑ |
117 | 80 |
X | 200t |
![]() =
= ![]()
x=292.5t
答:需要氯化钠的质量为292.5t。
【解析】解:(1)甲质子数为13,所以对应的是铝元素,在化合物中表现化合价为+3,价,而乙是氧元素,在化合物中一般表现为﹣2价,形成的化合物为氧化铝,两者反应的化学方程式为:4Al+3O2═2 Al2O3;(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.根据铁和硫酸铜溶液和质量守恒定律可推测,生成气体应该为氢气. A.产生的气体可能是H2 , 根据分析可知,正确;
B.由于铁和硫酸铜溶液均不含碳元素,根据质量守恒定律可得,产生的气体不可能是CO2 . 错误;
C.根据金属和溶液反应生成氢气,可推测CuSO4溶液中可能含有少量的某种酸.正确;
D.既然含有酸,则CuSO4溶液的pH就 小于7.正确.
故选:B.(3)实验的目的是除去氯化钠中氯化钙,所以应该加入能够使钙沉淀且不引入新的杂质的物质,所以加入碳酸钠,而为了使氯化钙完全沉淀,所以加入的碳酸钠是过量的,所以需要进一步除去,也就是氯化钠中混有了碳酸钠,此时加入盐酸除去碳酸钠.
根据分析可得①试剂A的化学式为 Na2CO3 . ②加入足量稀盐酸的目的是 除去过量的碳酸钠.③操作Ⅰ是固液分离,为过滤,操作Ⅱ是可溶性物质和溶剂分离是蒸发;④操作Ⅰ、Ⅱ中都要用到一种玻璃仪器,该仪器在操作Ⅱ中的作用是 用玻璃棒不断搅拌,防止因局部温度过高,造成液滴飞溅(4)解:设需要氯化钠的质量为x
2NaCl+2 H2O | 2NaOH+H2↑+Cl2↑ |
117 | 80 |
X | 200t |
![]() =
= ![]()
x=292.5t
故答案为:(1)4Al+3O2═2 Al2O3;(2)B;(3)①Na2CO3;②除去过量的Na2CO3;③过滤;蒸发;④用玻璃棒不断搅拌,防止因局部温度过高,造成液滴飞溅;(4)292.5t
(1)根据结构示意图和元素信息确定对应元素为氧元素和铝元素,进而根据化合价书写其反应的化学方程式;(2)根据生成气体和质量守恒定律分析,由于铁和硫酸铜溶液中均不含碳元素,所以不可能生成二氧化碳;(3)实验的目的是除去氯化钠中氯化钙,所以应该加入能够使钙沉淀且不引入新的杂质的物质,所以加入碳酸钠,而为了使氯化钙完全沉淀,所以加入的碳酸钠是过量的,所以需要进一步除去,也就是氯化钠中混有了碳酸钠,此时加入盐酸除去碳酸钠.(4)根据氢氧化钠的质量和对应的化学方程式计算氯化钠的质量(也可以根据钠元素守恒用化学式求算).