题目内容
【题目】某化学兴趣小组在实验室完成以下实验任务:①制备纯净干燥的二氧化碳气体;②用一氧化碳气体测定某不纯氧化铁样品的纯度。试根据题目要求,回答下列问题(假定过程中所有发生的反应都恰好完全进行,硝酸银溶液可吸收HCl气体)
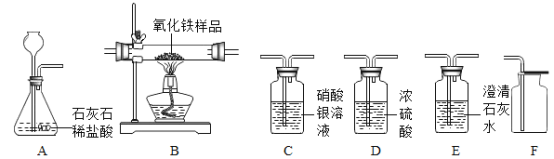
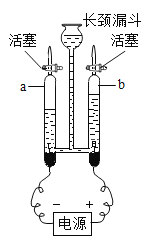
(1)若要制备并收集纯净干燥的二氧化碳,仪器的连接顺序为____;(填字母)
(2)装置A中发生反应的化学方程式为_____;
(3)欲用混有少量二氧化碳的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质。某同学所选仪器的连接顺序为:混合气体→B→E。
①若反应前装置B中样品质量为10g,反应后装置B中固体质量为7.9g,则样品中氧化铁的质量分数为_____。
②若用反应后装置E中增加的质量来计算样品中氧化铁的质量分数,结果将_____(选填“偏大”、“偏小”、“不受影响”之一),理由_____。
③从环境保护的角度考虑,针对该套实验装置不足提出的具体改进意见______。
【答案】ACDF CaCO3+2HCl=CaCl2+CO2↑+H2O 70% 偏大 原混合物中的二氧化碳也会被吸收 在装置末端加一个点燃的酒精灯处理尾气或用气球收集等
【解析】
(1)实验室用大理石与稀盐酸反应制取二氧化碳,由于盐酸是氯化氢气体的水溶液,所以制得的二氧化碳中往往混有氯化氢气体和水蒸气,硝酸银溶液能除去氯化氢气体;浓硫酸具有吸水性,除去水蒸气往往用浓硫酸,收集二氧化碳用向上排空气法,故若要制备并收集纯净干燥的二氧化碳,仪器的连接顺序为ACDF;
(2)装置A中发生反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)①设样品中氧化铁的质量分数为x。
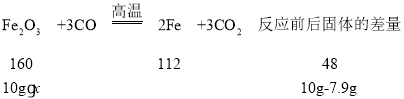
![]() 解得x=70%;
解得x=70%;
②由于原混合物中含有二氧化碳,反应后装置E中增加的质量是吸收二氧化碳的质量,此质量包括原混合物中含有的二氧化碳及生成的二氧化碳。故若用反应后装置E中增加的质量来计算样品中氧化铁的质量分数,结果将偏大,理由是原混合物中的二氧化碳也会被吸收。
③该装置没有处理尾气,尾气中含有的一氧化碳会污染空气,从环境保护的角度考虑,应该在装置末端增加一个点燃的酒精灯处理掉尾气或用气球收集等。

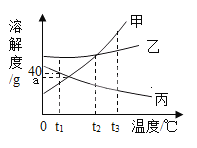
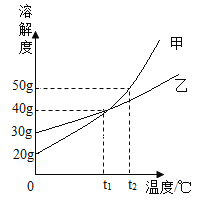
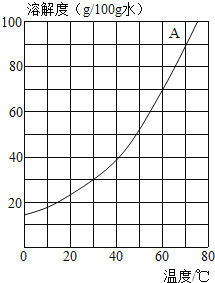
【题目】下图是A物质的溶解度曲线示意图,下表是B物质在不同温度时的溶解度表。
温度(°C) | B物质溶解度 (g/100g 水) |
0 | 32 |
20 | 35 |
40 | 40 |
60 | 45 |
80 | 55 |
①溶解度“表”和“图”各有优点,溶解度示意图的优点是__________。 50°C时,A物质的溶解度_________(选填“>” “<” “ = ”)B物质的溶解度。
②40°C时,向100g水中加入35g B物质,充分溶解后得到的是________(选填“饱和”、“不饱和”)溶液,此时溶液的质量分数为__________。
③20°C时,若要将质量分数为10%的A的不饱和溶液变为饱和溶液,写岀两种可以采用的方法是__________、_____________。
④对于20°C的A溶液与80°C的B溶液质量分数的分析,正确的是________(选填编号)
a 若两溶液的质量分数相等,则一定都为不饱和溶液
b 若两溶液的质量分数相等,则B溶液一定为不饱和溶液
c 若两溶液都为饱和溶液,则质量分数一定不相等
d 若A溶液为饱和溶液,则两溶液的质量分数一定不相等
【题目】分类、类比是初中化学常用的学习方法.
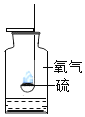
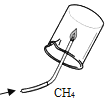
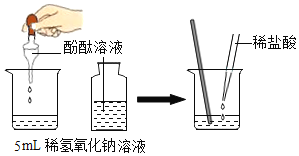
(1) 初中化学有许多实验,若按照实验目的分类,可将实验____________(填字母)分为一类;分类的依据是______________。
|
|
|
|
A水通电的实验 | B硫在氧气中燃烧实验 | C甲烷燃烧,罩一个内壁涂有澄清石灰水的烧杯 | D酸和碱能否发生反应的实验 |
(2)磷酸盐、磷酸氢盐的溶解性和碳酸盐相似,磷酸二氢盐和碳酸氢盐溶解性相似,则磷酸钡的溶解性为_____(填 “可溶”或“微溶”或“难溶”),碳酸钙可以和水、二氧化碳(看做碳酸)反应生成碳酸氢钙,请写出向磷酸钙固体中加入磷酸(H3PO4)溶液生成磷酸二氢盐反应的化学方程式_____________。