题目内容
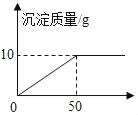
【题目】(4分)某校化学兴趣小组的同学取60g氯化钙(CaCl2)溶液,向其中加入适量碳酸钠(Na2CO3)溶液,反应完毕后过滤,所得固体用作制取牙膏摩擦剂的主要原料,同时所得滤液用来进行小麦选种(选种液要求氯化钠是质量分数在10%~20%之间)。实验过程中所加碳酸钠溶液的质量与生成碳酸钙沉淀的质量关系如图所示。通过如图可知:
(1)当氯化钙恰好反应完时:消耗碳酸钠溶液的质量为_____g;
(2)请通过计算回答,此时所得氯化钠溶液的质量分数是多少_____?能否用作小麦选种_____?
【答案】5011.7%此时所得氯化钠溶液的质量分数是11.7%,此时所得的氯化钠溶液可作为小麦选种液
【解析】
(1)根据图象可知到达最高点已经反应完了,消耗碳酸钠溶液质量为50g,改成横线时说明沉淀不再增加,所以生成沉淀10g;
(2)设当氯化钙反应完全时,生成氯化钠的质量为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
100 117
10g x
![]() ,x=11.7g,反应后溶液质量为:60g+50g-10g=100g,所以氯化钠溶液的质量分数为
,x=11.7g,反应后溶液质量为:60g+50g-10g=100g,所以氯化钠溶液的质量分数为![]() ×100%=11.7%;因为11.7%在10%-20%之间所以能作为小麦选种液,此时所得的氯化钠溶液可作为小麦选种液。
×100%=11.7%;因为11.7%在10%-20%之间所以能作为小麦选种液,此时所得的氯化钠溶液可作为小麦选种液。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目