题目内容
【题目】(8分)某兴趣小组同学为了验证铁和铜的金属活动性强弱,进行了如下的实验研究,请你回答有关问题:
[实验探究]
(1)甲同学设计的实验方案:取用砂纸打磨过的铁丝插入到盛有硫酸铜溶液的试管中,过一会儿取出铁丝,观察到铁丝表面_____________,得出结论铁比铜活动性强。
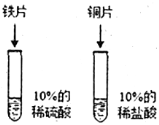
(2)乙同学设计的方案:(实验中所用铜片,铁片大小形状相同,且表面洁净光亮)
实验步骤 | 实验现象 | 实验结论 |
| 铜片的表面无气泡产生 铁片的表面有气泡产生 | 铁比铜的活动性强 |
[讨论交流]
(1)铁片与稀硫酸反应一段时间后溶液中可能含有的溶质是______________。
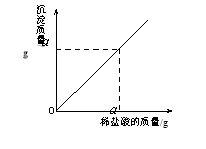
(2)实验前乙同学在配置10%的稀盐酸时,用到的仪器有烧杯、量筒、胶头滴管,还缺少的一种仪器是______________。在量取蒸馏水的体积时,若仰视读数,则会导致盐酸的溶质质量分数_________10%(填“>”“<”、“=”)
[反思评价]
你认为乙同学的方案__________(填“合理”或“不合理”),理由是:______________
[拓展应用]
农药波尔多液的主要成分是硫酸铜,不能用铁制容器盛放波尔多液的原因是:
____________________________________(用化学方程式表示)
【答案】(1)出现红色固体 (2)硫酸或H2SO4 (3)玻璃棒 < 不合理 反应用的酸的种类不同
(4)Fe+CuSO4=FeSO4+Cu
【解析】
试题分析:[实验探究](1)铁的活动性比铜强,可将铜从其盐溶液(硫酸铜溶液)中置换出来,生成铜单质。所以可观察到铁丝表面出现红色固体。
[讨论交流](1)铁片与稀硫酸反应会生成硫酸亚铁和氢气;反应一段时间后,溶液中一定存在硫酸亚铁。如硫酸未完全参与反应,则可能含有硫酸。
(2)配制稀盐酸时,要用到烧杯、量筒、胶头滴管和玻璃棒。在量取蒸馏水的体积时,若仰视读数,则会导致所量取水的体积偏小,则所得的盐酸的溶质质量分数会偏小。
[反思评价]乙同学的方案不合理,理由是:反应用的酸的种类不同,无法进行对比。
[拓展应用]如用铁制容器盛放波尔多液,由于铁的活动性比铜强,则铁会和硫酸铜反应生成铜和硫酸亚铁。会导致药效降低。

【题目】对下列生话中的现象或做法的解释正确的是
事 实 | 解 释 | |
A. | 蜡烛一吹就熄 | 吹出的CO2隔绝了氧气 |
B. | 热胀冷缩 | 分子间空隙随温度的改变而改变 |
C. | 食盐水可以导电 | 溶液中有自由移动的分子 |
D. | 伍德合金可作为保险丝 | 合金的熔点比其组成金属高 |