题目内容
下列配制的溶液浓度偏高的是( )
| A、配制盐酸溶液用量筒量取盐酸时俯视刻度线 |
| B、配制盐酸溶液定容时,仰视容量瓶刻度线 |
| C、称量4g NaOH 配制0.1mol/L NaOH溶液1000mL时,砝码错放左盘 |
| D、H2SO4稀释后未经冷却即注入容量瓶配制 |
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据c=
分析操作对溶质的物质的量或对溶液的体积是否有影响判断,如果n偏大或V偏小,则所配制溶液浓度偏高.
| n |
| V |
解答:解:
A、用量筒量取盐酸时俯视刻度线,所取盐酸的体积偏少,溶质的质量偏少,导致配制溶液的浓度偏低,故A错误;
B、定容时,仰视容量瓶刻度线,溶液的体积偏大,导致配制溶液的浓度偏低,故B错误.
C、称量40gNaOH固体时未用到游码,所以称量的氢氧化钠的质量和砝码的质量相等,对配制溶液的浓度无影响,故C错误.
D、硫酸稀释后未经冷却即注入容量瓶配制导致溶液的体积偏小,配制溶液的浓度偏高,故D正确.
答案:D.
A、用量筒量取盐酸时俯视刻度线,所取盐酸的体积偏少,溶质的质量偏少,导致配制溶液的浓度偏低,故A错误;
B、定容时,仰视容量瓶刻度线,溶液的体积偏大,导致配制溶液的浓度偏低,故B错误.
C、称量40gNaOH固体时未用到游码,所以称量的氢氧化钠的质量和砝码的质量相等,对配制溶液的浓度无影响,故C错误.
D、硫酸稀释后未经冷却即注入容量瓶配制导致溶液的体积偏小,配制溶液的浓度偏高,故D正确.
答案:D.
点评:本题考查配制一定物质的量浓度的溶液的误差分析,题目难度中等,注意根据c=
分析不当操作对n或V的影响.
| n |
| V |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
水受热变成水蒸气是由于( )
| A、水分子被破坏 |
| B、水发生了化学变化 |
| C、水分子之间的间隔变大 |
| D、水分子本身的体积变大 |
下列气体遇到明火可能爆炸的是( )
| A、氧气和氮气 |
| B、氢气和氮气 |
| C、纯净的氢气 |
| D、氧气和氢气 |
以下实验基本操作正确的是( )
A、 加热液体 |
B、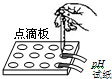 测定溶液pH |
C、 称量固体 |
D、 稀释浓硫酸 稀释浓硫酸 |
下列变化属于分解反应的是( )
A、氢气+氧化铜
| ||
B、氧气+氢气
| ||
C、碳酸钙
| ||
D、酒精+氧气
|
用量筒量取10mL水时仰视读数,则所量水的实际体积是( )
| A、10mL |
| B、大于10mL |
| C、小于10mL |
| D、无法确定 |
下列对实验现象的描述正确的是( )
| A、红磷在空气中燃烧产生大量白雾 |
| B、蜡烛在空气中燃烧生成二氧化碳和水 |
| C、铁丝在氧气中燃烧时火星四射、生成黑色固体 |
| D、硫在空气中燃烧生成有刺激性气味的二氧化硫 |
这里的钙、镁、钾、钠指的是( )
| A、元素 | B、原子 | C、分子 | D、单质 |
 如图所示,向小试管中分别放入下列一定量的物质后:
如图所示,向小试管中分别放入下列一定量的物质后: