题目内容
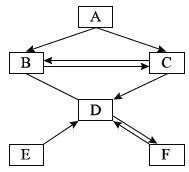
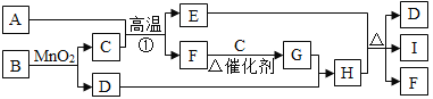
【题目】在下图所示的物质转化关系中(反应物生成物均已给出),A为某种含硫矿物的主要成分且A中硫元素的质量分数为20%,反应①是工业上冶炼金属的一种方法。B、D、F、G是氧化物。C、E是单质,I的溶液呈蓝色。
(1)A的化学式为_________________;
(2)G的化学式为_________________;
(3)E与H的浓溶液反应的化学方程式_____________________________________________;
(4)I的溶液与氢氧化钠溶液反应的化学方程式_______________________________________。
【答案】 Cu2S SO3 Cu +2H2SO4(浓)==CuSO4+ H2O+SO2↑ CuSO4 +2NaOH==Cu(OH)2↓+Na2SO4
【解析】B在二氧化锰的催化下分解生成C和D,且B、D是氧化物,C是单质,故B是过氧化氢,D是水,C是氧气。由I的溶液呈蓝色可知,I中含有铜元素,而I中的铜元素应来自于A,而A为某种含硫矿物的主要成分且A中硫元素的质量分数为20%,故A是Cu2S;Cu2S与O2在高温的条件下反应生成Cu和SO2,又E是单质,F是氧化物,故E是Cu,F是SO2;二氧化硫与氧气在有催化剂并加热的条件下反应生成三氧化硫,又G是氧化物,故G是SO3;三氧化硫与水反应生成硫酸,故H是硫酸;硫酸与铜在加热的条件下反应生成硫酸铜、水、二氧化硫,故I是硫酸铜。(1)A的化学式为 Cu2S;(2)G的化学式为SO3;(3)E与H的浓溶液反应的化学方程式为Cu +2H2SO4(浓)=CuSO4+ H2O+SO2↑;(4)I的溶液与氢氢氧化钠溶液反应的化学方程式为CuSO4 +2NaOH=Cu(OH)2↓+Na2SO4。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案