题目内容
不能用作证明质量守恒定律实验的装置是( )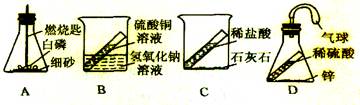
C
解析试题分析:验证质量守恒定律:当有气体参与或生成时,需在密闭容器中进行;没有气体参与或生成的反应在密闭或敞口容器中进行,均可得出正确的结论。故选C,稀盐酸和石灰石反应有二氧化碳生成,验证质量守恒定律,需在密闭容器中进行。
考点:质量守恒定律

练习册系列答案
相关题目
下列变化中,氢元素由化合态变成游离态的是( )
| A.电解水 | B.燃烧氢气 | C.氢气液化 | D.碳酸分解 |
化学方程式是重要的化学用语,下列化学方程式符合题意且书写正确的是( )
A.医疗上用氢氧化镁治疗胃酸过多:Mg(OH)2 +HCl 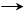 MgCl2 +H2O MgCl2 +H2O |
B.正常雨水的值约为⒌6的原因:CO2 +H2O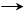 H2CO3 H2CO3 |
C.证明铁是金属活动性顺序表中氢之前的金属:2Fe + 6HCl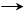 2 FeCl3 + 3 H2↑ 2 FeCl3 + 3 H2↑ |
D.发射火箭时用液氢作燃料:2 H2 + O2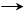 2H2O 2H2O |
物质的俗称与其化学式不相符合的是( )
| A.食盐 NaCl | B.生石灰 Ca(OH)2 |
| C.烧碱 NaOH | D.胆矾 CuSO4·5H2O |
某物质在空气中完全燃烧,测得生成物只含有二氧化碳、水蒸气、二氧化硫,对该物质的推断正确的是
| A.一定含有碳、氢、硫元素 | B.一定含有碳、氢、氧元素 |
| C.只含有碳、氢元素 | D.一定含有碳、氢、氧,可能含有硫元素 |
醋酸、甲醛的化学式依次是C2H4O2、CH2O,关于它们的说法正确的是
| A.任意比混合二种化合物并溶解于水,所得混合液中H、O元素质量比无法确定 |
| B.任意比混合二种化合物并溶解于水,所得混合液中H、O元素质量比是定值 |
| C.任意比混合二种化合物,完全燃烧产生的二氧化碳与水的质量比是22:9 |
| D.任意比混合二种化合物,完全燃烧产生的二氧化碳与水的质量比无法确定 |
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是 ( )
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
A.该变化的基本反应类型是分解反应
B.反应后物质M的质量为l3g
C.反应中N、P的质量比为5:4
D.物质Q可能是该反应的催化剂
下列化学方程式正确的是
| A.铁屑溶于稀硫酸:2Fe+3H2SO4═Fe2(SO4)3+3H2↑ |
| B.食盐溶于硝酸钾溶液:NaCl+KNO3═NaNO3+KCl |
| C.用稀盐酸除去铁制品表面的铁锈:2HCl+FeO═FeCl2+H2O |
| D.向纯碱溶液中滴加氯化钙溶液:Na2CO3+CaCl2═CaCO3↓+2NaCl |
根据氨碱法用食盐制纯碱的反应原理是:
(1)NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(2)2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
下列对上述信息的有关理解中,错误的是( )
| A.用食盐制纯碱需要含碳、氧元素的物质 |
| B.纯碱属于盐类物质 |
| C.因生成气体,反应不遵循质量守恒定律 |
| D.副产品氯化铵是一种氮肥 |