题目内容
【题目】请结合下列实验常用装置,回答有关问题。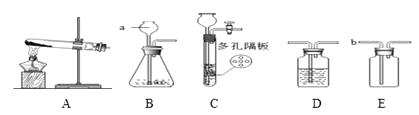
(1)写出图中标有字母的仪器的名称:a。
(2)若用A装置制氧气,其反应的化学方程式为 , 在制取氧气时试管中的棉花没有发生燃烧,根据燃烧的条件分析,其主要原因是。
(3)若要制取二氧化碳,应选用的发生装置是(填“A”或“B”)。其化学方程式为 。若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放(填写试剂名称)。
(4)实验室常使用仪器E来收集气体,如现在要收集氢气,则气体从端进入(填“b”或“c”),有同学认为只要经过一定的改进措施,氧气也能从该端进入收集,则他的改进措施是。
(5)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置,当反应进行过程中,关闭该装置中的止水夹后,可以观察到的现象是。
【答案】
(1)长颈漏斗
(2)2KMnO4![]() K2MnO4+MnO2+O2↑,温度没有达到着火点
K2MnO4+MnO2+O2↑,温度没有达到着火点
(3)B,CaCO3+2HCl=CaCl2+CO2↑+H2O,浓硫酸
(4)C,瓶中装满水或将装置倒立放置
(5)液体下降与固体分离,反应停止
【解析】(1). 长颈漏斗 (2).发生装置中有棉花,说明是高锰酸钾法制氧气,方程式为 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ 燃烧需要同时具备的三个条件:物质有可燃性、温度达可燃物的着火点、与氧气充分接触;在制取氧气时试管中的棉花没有发生燃烧,其主要原因是温度没有达到着火点 (3). 食盐水蒸发石灰石和稀盐酸反应制取二氧化碳,应选用的发生装置固液常温型B 。方程式为 CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O ; 应该用浓硫酸干燥二氧化碳 (4). 氢气的密度比空气小,应从C 进入 ; 氧气的密度比空气大,收集氧气时将装置倒立放置 ,或瓶中装满水。 (5). 关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。
K2MnO4 + MnO2 + O2↑ 燃烧需要同时具备的三个条件:物质有可燃性、温度达可燃物的着火点、与氧气充分接触;在制取氧气时试管中的棉花没有发生燃烧,其主要原因是温度没有达到着火点 (3). 食盐水蒸发石灰石和稀盐酸反应制取二氧化碳,应选用的发生装置固液常温型B 。方程式为 CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O ; 应该用浓硫酸干燥二氧化碳 (4). 氢气的密度比空气小,应从C 进入 ; 氧气的密度比空气大,收集氧气时将装置倒立放置 ,或瓶中装满水。 (5). 关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。
所以答案是:长颈漏斗、2KMnO4![]() K2MnO4+MnO2+O2↑、B、CaCO3+2HCl=CaCl2+CO2↑+H2O、浓硫酸、C、瓶中装满水或将装置倒立放置、液体下降与固体分离,反应停止。
K2MnO4+MnO2+O2↑、B、CaCO3+2HCl=CaCl2+CO2↑+H2O、浓硫酸、C、瓶中装满水或将装置倒立放置、液体下降与固体分离,反应停止。

 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】某兴趣小组用下图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g。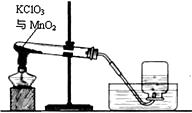
加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(1)氧气的相对分子质量=。
(2)共制得氧气g。
(3)计算所得氯化钾溶液的溶质质量分数。