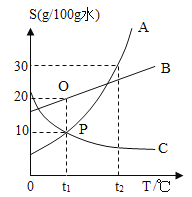
题目内容
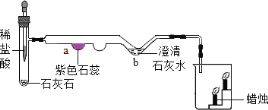
【题目】高级汽车中常配置有一种汽车安全气袋,内部贮存有硝酸铵。当汽车变速行驶中受到猛烈撞击时,硝酸铵迅速分解产生大量的一氧化二氮(N2O)气体和另一种氧化物充满气袋,填补在乘员与挡风玻璃,方向盘之间,防止乘员受伤。
(1)NH4NO3受撞击后发生分解反应的化学方程式是_____。
(2)上面的反应中,反应物和生成物中氮元素的化合价从左到右依次为_____。
【答案】NH4NO3![]() N2O↑+2H2O -3;+5;+1
N2O↑+2H2O -3;+5;+1
【解析】
(1)根据质量守恒定律可以知道:化学反应中元素的种类不变,反应物中含有氢元素,因此另一种氧化物中应该含有氢元素,所以含氢元素的氧化物是水;因此硝酸铵在撞击条件下反应生成一氧化二氮和水;该反应的化学方程式为:NH4NO3![]() N2O↑+2H2O;
N2O↑+2H2O;
(2)设铵根中氮元素的化合价为x,x+(+1)×4=+1,x=-3;
设硝酸根中氮元素的化合价为y,y+(-2)×3=-1,y=+5;
设一氧化二氮中氮元素的化合价为z,z×2+(-2)=0,z=+1。

【题目】金属锰(Mn)及其化合物用途广泛。铁锰合金(锰钢)可用作大型体育场馆的网封架屋顶材料、铁轨、桥梁等。部分锰的化合物颜色及溶解性见下表,回答下列问题。
物质 | KMnO4 | MnO2 | MnSO4 | Mn(OH)2 | MnO(OH)2 |
颜色 | 暗紫色 | 黑色 | 白色 | 白色 | 棕色 |
溶解性 | 易溶 | 难溶 | 易溶 | 难溶 | 难溶 |
(1)KMnO4广泛用作医药杀菌剂和防臭剂,也可用于实验室制备氧气,该反应化学方程式为______。
(2)将适当比例的铁矿石(Fe2O3)、软锰矿(MnO2)、焦炭混合加入高炉,通入热空气熔炼可得到铁锰合金。用化学方程式表示生成金属锰的过程:①C+O2![]() CO2;②______;③MnO2+2CO
CO2;②______;③MnO2+2CO![]() Mn+2CO2。
Mn+2CO2。
(3)已知:①MnSO4+2NaOH=Mn(OH)2↓+Na2SO4②2Mn(OH)2+O2=2MnO(OH)2若向盛有MnSO4溶液的试管中加入少量NaOH溶液,静置,可观察到的现象是______。