题目内容
某工厂用Ca(OH)2处理含HCl的废水,若该厂每天排放20t HCl的质量分数为0.3%的废水,请通过计算说明每天所需Ca(OH)2的质量是多少吨(精确到0.01t).
解:设处理此废水需固体Ca(OH)的质量为X
HCl的质量为:20t×0.3%=0.06t
2HCl+Ca(OH)2═CaCl2+2H2O
73 74
0.06t X
 =
=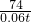
 =
= X≈0.06t
X≈0.06t
答:处理此废水需固体Ca(OH)的质量为0.06t.
故答案为:0.06t
分析:可以根据提供的信息进行分析、判断,从而得出正确的结论.根据废水的质量和HCl的质量分数求出HCl的质量,在根据化学方程式可以求出Ca(OH)2的质量.
点评:解答本题的关键是要充分理解相关方面的计算方法和节能环保的重要性,只有这样才能对问题做出正确的判断
HCl的质量为:20t×0.3%=0.06t
2HCl+Ca(OH)2═CaCl2+2H2O
73 74
0.06t X
 =
=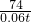
 =
= X≈0.06t
X≈0.06t答:处理此废水需固体Ca(OH)的质量为0.06t.
故答案为:0.06t
分析:可以根据提供的信息进行分析、判断,从而得出正确的结论.根据废水的质量和HCl的质量分数求出HCl的质量,在根据化学方程式可以求出Ca(OH)2的质量.
点评:解答本题的关键是要充分理解相关方面的计算方法和节能环保的重要性,只有这样才能对问题做出正确的判断

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目